题目内容
9.在盛有1mL 1mol•L-1AlCl3溶液的试管中加入2mL10%的NH4F溶液,再加入1mL 3mol•L-1氨水,没有生成白色沉淀,其原因是( )| A. | 溶液的碱性太弱 | B. | Al3+不与氨水反应 | ||
| C. | 生成的Al(OH)3溶解了 | D. | Al3+几乎都与F-结合生成了新物质 |
分析 铝离子与氨水反应生成氢氧化铝沉淀,结合无沉淀生成来解答.
解答 解:因铝离子与氨水反应生成氢氧化铝沉淀,如果不加NH4F会产生沉淀,无沉淀产生,则必有F-影响,只能为F-具有强结合能力,Al3+几乎都与F-结合生成了新物质,再加氨水不生成沉淀,
故选D.
点评 本题考查物质的性质及反应,为高频考点,把握习题中的信息及沉淀生成的条件为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
7.下列各组离子在指定的溶液中,-定能大量共存的是( )
| A. | 在含有大量AlO2-的溶液中:Fe3+、Na+、NO3-、Cl- | |
| B. | 使淀粉碘化钾试纸变蓝的溶液中:K+、S2-、Cl-、HCO3- | |
| C. | 滴入KSCN溶液显红色的溶液中:K+、Fe2+、SO42-、Cl- | |
| D. | 与金属铝反应只能放出氢气的溶液中:NH4+、Cl-、Na+、NO3- |
8.高能糖电池是一种新型的电池,该电池解决了环境污染问题,有望在未来代替传统电池.该电池的工作原理为C6H12O6(葡萄糖)+6O2═6CO2+6H2O,下列有关说法正确的是( )
| A. | 该电池的工作环境应在高温条件下 | |
| B. | 正极反应:O2+4H++4e-═2H2O | |
| C. | 电池工作时葡萄糖在负极上失去电子发生还原反应 | |
| D. | 电池工作时H+由负极移向正极,但电解液的pH不变 |
5.有机物的结构可用“键线式”表示,如:CH3-CH═CH-CH3的键线式为  .已知有机物X的键线式为
.已知有机物X的键线式为 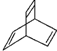 ,Y是X的同分异构体且属于芳香烃.下列关于Y的说法正确的是( )
,Y是X的同分异构体且属于芳香烃.下列关于Y的说法正确的是( )
 .已知有机物X的键线式为
.已知有机物X的键线式为  ,Y是X的同分异构体且属于芳香烃.下列关于Y的说法正确的是( )
,Y是X的同分异构体且属于芳香烃.下列关于Y的说法正确的是( )| A. | Y的结构简式为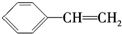 | |
| B. | Y能使溴水褪色,且反应后的混合液静置后不分层 | |
| C. | Y不能发生取代反应 | |
| D. | Y分子中的所有原子一定共面 |
4.美国通用原子能公司(GA)提出的碘硫热化学循环是由反应Ⅰ、Ⅱ、Ⅲ三步反应组成的(如图所示),下列有关说法正确的是( )


| A. | 设计该循环是为了制取能源气体O2 | |
| B. | 整个循环过程中产生1mol O2的同时产生44.8LH2 | |
| C. | 图中反应Ⅰ、Ⅱ、Ⅲ均为氧化还原反应 | |
| D. | 图中反应Ⅰ、Ⅱ、Ⅲ均可在常温常压下进行 |
14.下列实验操作简便、科学且易成功的是( )
| A. | 将乙酸和乙醇的混合液注入浓硫酸中制备乙酸乙酯 | |
| B. | 将铜丝在酒精灯外焰上加热变黑后再移至内焰,铜丝恢复原来的红色 | |
| C. | 在试管中注入2 mL CuSO4溶液,再滴几滴NaOH溶液后,加入乙醛溶液即有红色沉淀生成 | |
| D. | 向苯酚溶液中滴加几滴稀溴水出现白色沉淀 |
18.反应C+H2O$\stackrel{高温}{?}$CO+H2在密闭容器中进行.下列关于该反应的说法不正确的是( )
| A. | 降低温度能减慢反应速率 | |
| B. | 单质碳的颗粒变小能加快反应速率 | |
| C. | 增大H2O蒸气的浓度能加快反应速率 | |
| D. | 加入足量的C能使H2O反应完全 |
19.X、Y、Z、W为短周期主族元素,X原子M层有1个电子,Y原子最外层电子数为最内层电子数的2倍,Z元素的最高化合价为最低化合价绝对值的3倍,Z、W同周期,W的原子半径小于Z.下列叙述正确的是( )
| A. | 原子半径由大到小的顺序:Z、X、Y | |
| B. | 元素非金属性由强到弱的顺序:W、Z、Y | |
| C. | 简单气态氢化物的稳定性由强到弱的顺序:Z、W | |
| D. | W分别与X、Y形成的化合物化学键类型相同 |
