题目内容
(9分)下表是不同温度下水的离子积数据:
温度/℃ | 25 | t1 | t2 |
Kw/ mol2·L-2 | 1×10-14 | a | 1×10-12 |
试回答以下几个问题:
(1)若25< t1< t2,则a 1×10-14(填“<”、“>”或“=”),由此判断的理由是:
。
(2)在t1℃下,pH=10的NaOH溶液中,水电离产生的[OH-]为: 。
(3)在t2℃下,将pH=11的苛性钠溶液V1 L与pH=1的硫酸溶液V2 L混合(设混合后溶液体积为原两溶液体积之和)所得溶液的pH=2,则V1︰V2 = ,此溶液中各种离子的浓度由大到小的顺序是 。
(1) > 升高温度,水的电离程度增大,离子积增大 (2)1×10-10 mol·L-1
(3)9︰11 c(Na+)> c(SO42-)> c(H+)> c(OH-)
【解析】
试题分析:(1)升高温度,水的电离平衡正向移动,故水的离子积增大,所以a>1×10-14;(2)在t1℃下,pH=10的NaOH溶液中,[H+]=1×10-10,所以,由水电离的[OH-]为1×10-10;(3)t2℃下,将pH=11的苛性钠溶液,[OH-]为0.1 mol·L-;pH=1的硫酸溶液[H+]=0.1 mol·L-,所得溶液的pH=2, ,V1︰V2 =9:11,溶液中离子浓度为c(Na+)> c(SO42-)> c(H+)> c(OH-)。
,V1︰V2 =9:11,溶液中离子浓度为c(Na+)> c(SO42-)> c(H+)> c(OH-)。
考点:本题考查水的电离和溶液PH。

 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案通常人们把拆开1 mol某化学键所消耗的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热。
化学键 | Si—O | Si—Cl | H—H | H—Cl | Si—Si | Si—C |
键能/kJ·mol-1 | 460 | 360 | 436 | 431 | 176 | 347 |
工业上高纯硅可通过下列反应制取:SiCl4(g)+2H2(g) Si(s)+4HCl(g),该反应的反应热△H为
Si(s)+4HCl(g),该反应的反应热△H为
A.+236 kJ·mol-1 B.-236 kJ·mol-1
C.+412 kJ·mol-1 D.-412 kJ·mol-1
相同温度下,根据三种酸的电离平衡常数,下列判断正确的是
酸 | HX | HY | HZ |
Ka/mol·L-1 | 9×10-7 | 9×10-6 | 2×10-2 |
A.三种酸的强弱关系: HX>HY>HZ
B.反应 HZ+Y-===HY+Z-能够发生
C.相同温度下,0.1 mol?L?1的NaX、NaY、NaZ溶液,NaZ溶液pH最大
D.相同温度下,1 mol?L?1HX溶液的电离常数大于0.1 mol?L?1HX
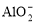 B.Cu2+ C.Al3+ D.Mg2+
B.Cu2+ C.Al3+ D.Mg2+ 2Fe2O3+4CO2。现煅烧464.0 kg的FeCO3,得到316.8 kg产品。若产品中杂质只有FeO,则该产品中Fe2O3的质量是 Kg。(摩尔质量/g·mol-1:FeCO3 116 Fe2O3 160 FeO 72)
2Fe2O3+4CO2。现煅烧464.0 kg的FeCO3,得到316.8 kg产品。若产品中杂质只有FeO,则该产品中Fe2O3的质量是 Kg。(摩尔质量/g·mol-1:FeCO3 116 Fe2O3 160 FeO 72)