题目内容
相同温度下,根据三种酸的电离平衡常数,下列判断正确的是
酸 | HX | HY | HZ |
Ka/mol·L-1 | 9×10-7 | 9×10-6 | 2×10-2 |
A.三种酸的强弱关系: HX>HY>HZ
B.反应 HZ+Y-===HY+Z-能够发生
C.相同温度下,0.1 mol?L?1的NaX、NaY、NaZ溶液,NaZ溶液pH最大
D.相同温度下,1 mol?L?1HX溶液的电离常数大于0.1 mol?L?1HX
B
【解析】
试题分析:电离平衡常数越大,酸性越强,故A错误;强酸能制取弱酸,故B正确;酸性越弱,酸根离子水解程度越大,相同温度下,0.1 mol?L?1的NaX、NaY、NaZ溶液,NaX溶液pH最大,故C错误;电离常数只与温度有关,故D错误。
考点:本题考弱电解质电离。

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
(9分)下表是不同温度下水的离子积数据:
温度/℃ | 25 | t1 | t2 |
Kw/ mol2·L-2 | 1×10-14 | a | 1×10-12 |
试回答以下几个问题:
(1)若25< t1< t2,则a 1×10-14(填“<”、“>”或“=”),由此判断的理由是:
。
(2)在t1℃下,pH=10的NaOH溶液中,水电离产生的[OH-]为: 。
(3)在t2℃下,将pH=11的苛性钠溶液V1 L与pH=1的硫酸溶液V2 L混合(设混合后溶液体积为原两溶液体积之和)所得溶液的pH=2,则V1︰V2 = ,此溶液中各种离子的浓度由大到小的顺序是 。

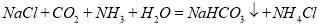 ”是“侯氏制碱法”的重要反应。下面是4位同学对该反应涉及的有关知识发表的部分见解。其中不正确的是
”是“侯氏制碱法”的重要反应。下面是4位同学对该反应涉及的有关知识发表的部分见解。其中不正确的是