题目内容
下列说法正确的是
A.氯化钾溶液在电流作用下电离成钾离子和氯离子
B.二氧化硫的水溶液能导电,故二氧化硫是电解质
C.硫酸钡难溶于水,所以硫酸钡属弱电解质
D.纯净的强电解质在液态时,可能导电
D
【解析】
试题分析:A.氯化钾溶液在水中或熔化状态下电离成钾离子和氯离子,错误;B.二氧化硫的水溶液能导电,是由于二氧化硫与水反应产生了亚硫酸,亚硫酸电离产生自由移动的离子,故亚硫酸是电解质,错误;C.硫酸钡难溶于水,但是溶于水的硫酸钡完全电离产生自由移动的离子,所以硫酸钡属强电解质,错误;D.纯净的强电解质若是离子化合物则在液态时能导电,若是共价化合物,则在液体是不能导电,正确。
考点:考查电解质的导电性与电解质的强弱及物质分类的关系的知识。

练习册系列答案
 导学全程练创优训练系列答案
导学全程练创优训练系列答案
相关题目
(9分)下表是不同温度下水的离子积数据:
温度/℃ | 25 | t1 | t2 |
Kw/ mol2·L-2 | 1×10-14 | a | 1×10-12 |
试回答以下几个问题:
(1)若25< t1< t2,则a 1×10-14(填“<”、“>”或“=”),由此判断的理由是:
。
(2)在t1℃下,pH=10的NaOH溶液中,水电离产生的[OH-]为: 。
(3)在t2℃下,将pH=11的苛性钠溶液V1 L与pH=1的硫酸溶液V2 L混合(设混合后溶液体积为原两溶液体积之和)所得溶液的pH=2,则V1︰V2 = ,此溶液中各种离子的浓度由大到小的顺序是 。

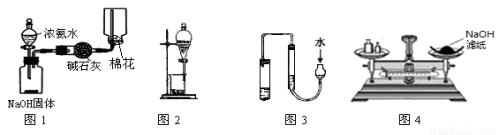
 和
和 的说法中正确的是
的说法中正确的是