题目内容
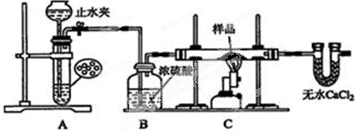
15. 有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取.纯净的A为无色黏稠液体,易溶于水.为研究A的组成与结构,进行了如下实验:
有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取.纯净的A为无色黏稠液体,易溶于水.为研究A的组成与结构,进行了如下实验:(1)称取A 9.0g,升温使其汽化,测其密度是相同条件下H2的45倍.实验结论:A的相对分子质量为90.
(2)将此9.0g A在足量纯O2中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重5.4g和13.2g.则A的分子式为C3H6O3.
(3)另取A 9.0g,跟足量的NaHCO3粉末反应,生成2.24L CO2(标准状况),若与足量金属钠反应则生成2.24L H2(标准状况).实验结论:A中含有的官能团:-COOH、-OH.
(4)A的核磁共振氢谱如图:A的结构简式
 .
.(5)写出两分子的A形成环状化合物的化学方程式2
 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$ +2H2O.
+2H2O.
分析 (1)同温同压下,气体的密度之比等于相对分子质量之比,据此计算;
(2)浓硫酸增重7.2g为水的质量,碱石灰增重17.6g为二氧化碳质量,计算有机物、水、二氧化碳物质的量,进而计算n(H)、n(C),根据质量守恒确定是否含有O元素,根据元素守恒来确定有机物的分子式;
(3)能与足量的NaHCO3粉末反应,说明含有-COOH,根据生成的二氧化碳的物质的量确定-COOH数目,能与钠反应生成氢气,结合生成氢气的物质的量确定是否含有-OH及羟基数目;
(4)核磁共振氢谱图中有几个峰值则含有几种类型的等效氢原子,结合由A的分子式、含有的官能团及核磁共振氢谱书写其结构简式;
(5)A的结构简式: ,两分子的A形成环状化合物为
,两分子的A形成环状化合物为 ,为酯化反应.
,为酯化反应.
解答 解:(1)由其密度是相同条件下H2的45倍,可知A的相对分子质量为45×2=90,
故答案为:90;
(2)由题意可推知:n(A)=$\frac{9.0g}{90g/mol}$=0.1 mol,n(C)=n(CO2)=$\frac{13.2g}{44g/mol}$=0.3 mol,n(H)=2n(H2O)=2×$\frac{5.4g}{18g/mol}$=0.6 mol,
n(O)=$\frac{9g-0.3×12g-0.6×1g}{1g/mol}$=0.3 mol,
所以A的分子式为:C3H6O3,
故答案为:C3H6O3;
(3)0.1 mol A与NaHCO3反应放出0.1 mol CO2,则说A中应含有一个羧基,而与足量金属钠反应则生成0.1 mol H2,说明A中还含有一个羟基,
故答案为:-COOH、-OH;
(4)核磁共振氢谱中有4个吸收峰,可知A中应含有4种不同环境的氢原子,A的结构简式为: ,
,
故答案为: ;
;
(5)A为 ,两分子的A形成环状化合物为
,两分子的A形成环状化合物为 ,则方程式为2
,则方程式为2 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$ +2H2O,
+2H2O,
故答案为:2 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$ +2H2O.
+2H2O.
点评 本题考查有机物的结构和性质,为高考常见题型,题目难度中等,侧重考查学生对知识的整合能力,注意掌握常见有机物结构与性质,根据A和碳酸氢钠、钠反应时生成气体体积判断含有的官能团类型为解答关键.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | Na2O2用作呼吸面具的供氧剂 | |
| B. | 工业上电解熔融状态的MgCl2制备Mg | |
| C. | 工业上利用合成氨实现人工固氮 | |
| D. | 实验室用NH4Cl和Ca(OH)2制备NH3 |
| A. | H2SO4溶液 | B. | AgNO3溶液 | C. | NaOH溶液 | D. | 氨水 |
| 第Ⅰ组 | 第Ⅱ组 | 第Ⅲ组 | |
| 甲 | BaCl2 | HCl | Cu(NO3)2 |
| 乙 | Fe2O3 | K2SO4 | H2SO4 |
| 丙 | Fe | NaOH | MgCl2 |
第Ⅲ组中有一种物质与第Ⅰ组中的所有物质反应,这种物质是H2SO4.
第Ⅱ组物质中,跟第Ⅰ组所有物质都不能发生反应的是NaOH.
(2)双氧水H2O2可作为矿业废液消毒剂,可以消除采矿业废液中的氰化物(如KCN)化学方程式为:KCN+H2O2+H2O═KHCO3+A↑(已配平)①生成物A的化学式为NH3;②反应中被氧化的元素为C;③该反应中的氧化剂是H2O2.
(3)写出下列物质在水溶液里的电离方程式:硫酸铁Fe2(SO4)3=2Fe3++3SO42-,氯酸钾KClO3=K++ClO3-,NaHSO4在熔融状态下的电离方程式是NaHSO4=Na++HSO4-.
(4)下列说法中正确的是BD.
A.NaHSO4属于酸 B.NaHSO4属于酸式盐
C.NaHSO4溶液属于电解质 D.NaHSO4溶液能与Zn反应生成氢气
(5)Fe(OH)3胶体的制备方法在沸腾的蒸馏水中加入饱和氯化铁溶液,当溶液变为红褐色时立即停止加热.
①混合物:铝热剂、碱石灰、水玻璃
②化合物:氯化钙、烧碱、胆矾
③酸性氧化物:Mn2O7、N2O3、SiO2
④碱性氧化物:Na2O2、CuO、Al2O3
⑤同素异形体:C60、C70、石墨⑥强电解质:BaSO4、MgO、Ba(OH)2.
| A. | ①②③⑤⑥ | B. | ②③④⑥ | C. | ①②④⑤ | D. | ①②④⑥ |
| A. | 1-丙醇与浓氢溴酸反应:CH3CH2 CH2OH+HBr$\stackrel{△}{→}$CH3CH2 CH2Br+H2O | |
| B. | 1-溴丙烷与氢氧化钠溶液共热:CH3CH2 CH2Br+NaOH$→_{△}^{水}$CH3CH2 CH2OH+NaBr | |
| C. | 苯酚钠中通入少量二氧化碳:2 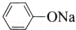 +CO2+H2O→2 +CO2+H2O→2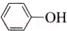 +Na2CO3 +Na2CO3 | |
| D. | 蔗糖在稀硫酸作用下水解:C12H22O11(蔗糖)+H2O$→_{△}^{稀硫酸}$C6H12O6(果糖)+C6H12O6(葡萄糖) |