题目内容
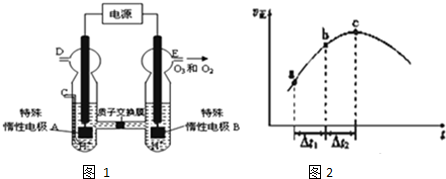
在一定温度下,将等量的气体分别通入起始体积相同的密闭容器I(恒容)和Ⅱ(恒压)中,使其发生反应,t.时容器I中达到化学平衡,x、Y、z的物质的量的变化如图所示,则下列有关推断正确的是( )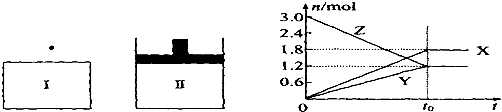

| A、该反应的化学方程式为:3X+2Y?3Z |
| B、若两容器中均达到平衡后,两容器的体积V(I)<V(Ⅱ),则容器Ⅱ达到平衡所用时间小于t |
| C、若两容器中均达到平衡时,两容器中Z的物质的量分数相同,则Y为固态或液态 |
| D、达平衡后,若对容器Ⅱ升高温度时其体积增大,说明Z发生的反应为吸热反应 |
考点:化学平衡建立的过程
专题:化学平衡专题
分析:A、根据反应中反应物减小,生成物增加,变化的物质的量之比等于计量数之比,写出方程式,据此判断;
B、根据压强对化学反应速率的影响判断;
C、根据平衡移动的影响因素判断;
D、根据温度对平衡移动的影响判断.
B、根据压强对化学反应速率的影响判断;
C、根据平衡移动的影响因素判断;
D、根据温度对平衡移动的影响判断.
解答:
解:A、根据图可知,反应中X增加了1.8mol,Y增加了1.2mol,Z减小了1.8mol,所以X、Y为生成物,Z为反应物,X、Y、Z的变化的物质的量之比为3:2:3,所以方程式为3Z?3X+2Y,故A错误;
B、若两容器中均达到平衡后,两容器的体积V(I)<V(Ⅱ),说明该反应是气体体积增大的反应,在反应过程中Ⅰ的压强大于Ⅱ的压强,所以Ⅰ中的反应速率快于Ⅱ,故容器Ⅱ达到平衡所用时间大于t,故B错误;
C、由于两容器一为恒压一为恒容,达到平衡时,两容器中Z的物质的量分数相同,说明压强对该反应的平衡没有影响,所以该反应前后气体的计量数应相等,结合方程式3Z?3X+2Y可知,Y为固态或液态,故C正确;
D、容器Ⅱ升高温度时其体积增大,不能说明Z发生的反应为吸热反应,因为Ⅱ是恒压容器,气体受热彭胀也能使体积增大,故D错误;
故选C.
B、若两容器中均达到平衡后,两容器的体积V(I)<V(Ⅱ),说明该反应是气体体积增大的反应,在反应过程中Ⅰ的压强大于Ⅱ的压强,所以Ⅰ中的反应速率快于Ⅱ,故容器Ⅱ达到平衡所用时间大于t,故B错误;
C、由于两容器一为恒压一为恒容,达到平衡时,两容器中Z的物质的量分数相同,说明压强对该反应的平衡没有影响,所以该反应前后气体的计量数应相等,结合方程式3Z?3X+2Y可知,Y为固态或液态,故C正确;
D、容器Ⅱ升高温度时其体积增大,不能说明Z发生的反应为吸热反应,因为Ⅱ是恒压容器,气体受热彭胀也能使体积增大,故D错误;
故选C.
点评:本题主要考查了根据图写化学方程式、影响平衡移动的因素等知识点,中等难度,解题的关键是对Y的状态的判断.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
分离NaCl、FeCl3和BaSO4的混合物,应选用的一组试剂是( )
| A、H2O、AgNO3、HNO3 |
| B、H2O、NaOH、HNO3 |
| C、H2O、NaOH、HCl |
| D、H2O、KOH、HNO3 |
下列各物质中所含的少量杂质,用括号内的物质能除去,并且不引进其他杂质的是 ( )
| A、二氧化碳中所含的氯化氢(NaOH溶液) |
| B、氢气中所含的硫化氢(硫酸铜溶液) |
| C、乙酸乙酯中所含的乙酸(乙醇) |
| D、氯化钠溶液中所含的氯化钡(硫酸) |