题目内容
18.①~⑧种元素在元素周期表中的位置如下图所示,回答下列问题:
(1)①~⑧元素中最不活泼的元素是Ar(填元素符号);
(2)②与④两元素形成的化合物的电子式为

(3)⑤⑥⑦三种元素原子半径由大到小的顺序排列为Na>Al>Cl(用元素符号表示);
(4)③、⑤两元素最高价氧化物对应的水化物在溶液中相互反应的化学方程式为NaOH+HNO3=NaNO3+H2O.
分析 由元素在周期表中的位置可知①为H元素、②为C元素、③为N元素、④为O元素、⑤为Na元素、⑥为Al元素、⑦为Cl元素、⑧为Ar元素.
(1)同周期元素中零族元素性质最不活泼;
(2)②与④两元素形成的化合物CO2;
(3)⑤⑥⑦位于同一周期,从左到右原子半径减小;
(4)③、⑤两元素最高价氧化物对应的水化物分别为硝酸、氢氧化钠,发生中和反应.
解答 解:(1)同周期元素中零族元素性质最不活泼,所以Ar的性质最不活泼,故答案为:Ar;
(2)②与④两元素形成的化合物CO2,为共价化合物,电子式为 ,故答案为:
,故答案为: ;
;
(3)⑤⑥⑦位于同一周期,从左到右原子半径减小,则原子半径大小顺序为Na>Al>Cl,
故答案为:Na>Al>Cl;
(4)③、⑤两元素最高价氧化物对应的水化物分别为硝酸、氢氧化钠,发生中和反应,反应的化学方程式为NaOH+HNO3=NaNO3+H2O,故答案为:NaOH+HNO3=NaNO3+H2O.
点评 本题考查结构性质位置关系应用,为高考常见题型和高频考点,侧重考查学生的分析能力,推断元素是解题关键,需要学生熟练掌握元素化合物结构与性质,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.下列实验操作中有错误的是( )
| A. | 1mol任何物质体积的大小取决于构成物质的粒子的大小和粒子之间的距离 | |
| B. | 分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 | |
| C. | 蒸馏中,冷却水应从冷凝管的下口通入,上口流出 | |
| D. | 蒸馏时,温度计水银球应浸没在液体中 |
9.目前全球掀起新一轮探月高潮.月球上蕴藏着丰富的氦-3(3He),用它可以给核聚变提供能源.关于3He的下列说法中正确的是( )
| A. | 3He与3H中含有相同的中子数 | |
| B. | 通过化学反应可以实现3He与4He的相互转化 | |
| C. | 1 mol氦气含有质子数为2 mol | |
| D. | 3He与4He互为同素异形体 |
13.下列反应中,属于取代反应的是( )
| A. | CH4$\stackrel{高温}{→}$C+2H2 | |
| B. | CH3CH═CH2+Br2$\stackrel{CCI_{1}}{→}$CH3CHBrCH2Br | |
| C. | CH4+2O2$\stackrel{点燃}{→}$CO2+2H2O | |
| D. | Cl2+C2H6$\stackrel{光}{→}$C2H5Cl+HCl |
10.一定温度下,将 2mol SO2 和 1mol O2充入一定容密闭容器中,在催化剂存在下进行下列反应:2SO2(g)+O2(g)?2SO3(g);△H=-197kJ/mol,下列说法中正确的是( )
| A. | 达到反应限度时,生成 SO3 为2 mol | |
| B. | 达到反应限度时,反应放出 197 kJ 的热量 | |
| C. | 达到反应限度时SO2、O2、SO3的分子数之比一定为2:1:2 | |
| D. | 达到反应限度时SO2的消耗速率必定等于SO3的消耗速率 |
7.对于有机物 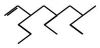 命名正确的是( )
命名正确的是( )
 命名正确的是( )
命名正确的是( )| A. | 5,7-二甲基-3-乙基-1-辛烯 | B. | 3-乙基-5,7-二甲基-1-壬烯 | ||
| C. | 3-甲基-5-乙基-7-丙基-8-壬烯 | D. | 7-甲基-5-乙基-3-丙基-1-壬烯 |
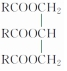 ”来表示,其中R为碳原子数目多于10的链烃基,可以相同也可以不同.分子式为C51H92O6的某油脂在稀硫酸中加热水解后得到A、B两种物质,若A的相对分子质量为92(已知:R1-CH═CH-R2$→_{H+}^{KMnO_{4}}$R1-COOH+R2-COOH),则
”来表示,其中R为碳原子数目多于10的链烃基,可以相同也可以不同.分子式为C51H92O6的某油脂在稀硫酸中加热水解后得到A、B两种物质,若A的相对分子质量为92(已知:R1-CH═CH-R2$→_{H+}^{KMnO_{4}}$R1-COOH+R2-COOH),则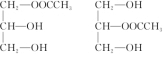 .
.