题目内容
14.下列反应符合图示的是( )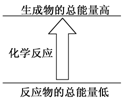
| A. | 镁片与盐酸的反应 | B. | Ba(OH)2•8H2O与NH4Cl晶体的反应 | ||
| C. | 酸碱中和反应 | D. | 乙醇在氧气中的燃烧反应 |
分析 根据图示可知,反应中反应物的总能量小于生成物的总能量,该反应是吸热反应,然后结合选项进行判断.
解答 解:根据图示可知:反应物的总能量小于生成物的总能量,所表示的反应为吸热反应,
A.铝片与盐酸的反应为放热反应,故A错误;
B.Ba(OH)2•8H2O与NH4Cl晶体的反应为吸热反应,故B正确;
C.酸碱中和反应为放热反应,故C错误;
D.乙醇在氧气中的燃烧为放热反应,故D错误.
故选B.
点评 本题考查反应热与焓变的应用,题目难度不大,明确化学反应与能量变化的关系为解答关键,注意掌握常见吸热反应、放热反应类型,试题培养了学生的灵活应用基础知识的能力.

练习册系列答案
 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案
相关题目
5.YBa2Cu8Ox(Y为元素钇)是磁悬浮列车中的重要超导材料,关于${\;}_{39}^{89}$Y的说法正确的是( )
| A. | Y 在周期表中的位置是第4周期ⅢB族 | |
| B. | 属于非金属元素 | |
| C. | 核素${\;}_{39}^{89}$Y的质子数与中子数之差为 50 | |
| D. | ${\;}_{39}^{89}$Y和${\;}_{39}^{90}$Y是两种不同的核素 |
2.温度为T时,向2.0L恒容密闭容器中充入1.0mol PCl5,反应PCl5(g)?PCl3(g)+Cl2(g)经过一段时间后达到平衡.反应过程中测定的部分数据见表:下列说法正确的是( )
| t/s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
| A. | 反应在前50s的平均速率v(Cl2)=0.0016 mol•L-1•min-1 | |
| B. | 保持其他条件不变,升高温度,平衡时c(PCl3)=0.11 mol•L-1,则该反应的△H<0 | |
| C. | 温度为T时,起始时向容器中充入1.0 mol PCl5、0.20 mol PCl3和0.20 mol Cl2,反应达到平衡前v(正)<v(逆) | |
| D. | 温度为T时,起始时向容器中充入0.5 mol PCl3和0.5 mol Cl2,达到平衡时,PCl3的转化率小于80% |
9.已知:
①2C(s)+O2(g)=2CO(g)△H=-220kJ•mol-1
②氢气燃烧的能量变化示意图:
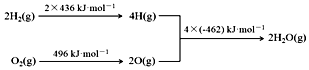
下列说法正确的是( )
①2C(s)+O2(g)=2CO(g)△H=-220kJ•mol-1
②氢气燃烧的能量变化示意图:

下列说法正确的是( )
| A. | C(s)+H2O(g)═CO(g)+H2(g)△H=+130 kJ•mol-1 | |
| B. | H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-480 kJ•mol-1 | |
| C. | C(s)燃烧热为110 kJ•mol-1 | |
| D. | 欲分解2 mol H2O(l),至少需要提供480kJ的热量 |
4.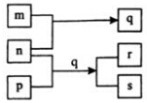 元素W、X、Y、Z的原子序数依次增加.p、q、r是由这些元素组成的二元化合物.m、n分别是元素Y、Z的单质,n通常为深红棕色液体,0.01mol/L r溶液的pH为2,p被英国科学家法拉第称为“氢的重碳化合物”,s通常是难溶于水、比水重的油状液体.上述物质的转化关系如图所示.下列说法错误的是( )
元素W、X、Y、Z的原子序数依次增加.p、q、r是由这些元素组成的二元化合物.m、n分别是元素Y、Z的单质,n通常为深红棕色液体,0.01mol/L r溶液的pH为2,p被英国科学家法拉第称为“氢的重碳化合物”,s通常是难溶于水、比水重的油状液体.上述物质的转化关系如图所示.下列说法错误的是( )
 元素W、X、Y、Z的原子序数依次增加.p、q、r是由这些元素组成的二元化合物.m、n分别是元素Y、Z的单质,n通常为深红棕色液体,0.01mol/L r溶液的pH为2,p被英国科学家法拉第称为“氢的重碳化合物”,s通常是难溶于水、比水重的油状液体.上述物质的转化关系如图所示.下列说法错误的是( )
元素W、X、Y、Z的原子序数依次增加.p、q、r是由这些元素组成的二元化合物.m、n分别是元素Y、Z的单质,n通常为深红棕色液体,0.01mol/L r溶液的pH为2,p被英国科学家法拉第称为“氢的重碳化合物”,s通常是难溶于水、比水重的油状液体.上述物质的转化关系如图所示.下列说法错误的是( )| A. | 原子半径的大小W<X<Z | B. | W的氧化物常温常压下为液态 | ||
| C. | Y的氧化物可能呈黑色或红棕色 | D. | Z的氧化物的水化物一定为强酸 |