题目内容
3.根据要求完成下列化学方程式或离子方程式(1)金属铝与氢氧化钠溶液反应2Al+2NaOH+2H2O═2NaAlO2+3H2↑;
(2)工业用焦炭与二氧化硅制粗硅2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑
(3)金属铝与氧化铁的铝热反应2A1+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+A12O3
(4)Na2O2与水反应的离子方程式2Na2O2+2H2O=4Na++4OH-+O2↑
(5)氯化亚铁溶液与氯气反应的离子方程式2Fe2++Cl2=2Fe3++2Cl-.
分析 (1)Al和NaOH溶液反应生成偏铝酸钠和氢气;
(2)工业用焦炭与二氧化硅反应生成硅与一氧化碳;
(3)金属铝与氧化铁的铝热反应生成氧化铝和单质铁;
(4)Na2O2与水反应生成氢氧化钠和氧气;
(5)氯化亚铁溶液与氯气反应生成氯化铁.
解答 解:(1)Al和NaOH溶液反应生成偏铝酸钠和氢气,化学方程式为2Al+2NaOH+2H2O═2NaAlO2+3H2↑,故答案为:2Al+2NaOH+2H2O═2NaAlO2+3H2↑;
(2)工业用焦炭与二氧化硅反应生成硅与一氧化碳,反应的化学方程式为:2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑,故答案为:2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑;
(3)金属铝与氧化铁的铝热反应生成氧化铝和单质铁,反应的化学方程式为:2A1+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+A12O3,故答案为:2A1+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+A12O3;
(4)Na2O2与水反应生成氢氧化钠和氧气,反应的离子方程式为:2Na2O2+2H2O=4Na++4OH-+O2↑,故答案为:2Na2O2+2H2O=4Na++4OH-+O2↑;
(5)氯化亚铁溶液与氯气反应生成氯化铁,反应的离子方程式为:2Fe2++Cl2=2Fe3++2Cl-,故答案为:2Fe2++Cl2=2Fe3++2Cl-.
点评 本题考查离子方程式和化学方程式的书写,明确反应实质是解本题关键,知道离子方程式书写规则,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
13.标准状况下,将aL由H2和Cl2组成的混合气体点燃,充分反应后,将混合气体通入足量的NaOH溶液中,气体被完全吸收,则原混合气体中Cl2的体积至少为( )
| A. | $\frac{a}{2}$L | B. | $\frac{a}{3}$L | C. | $\frac{a}{4}$L | D. | $\frac{a}{5}$L |
14.下列反应符合图示的是( )
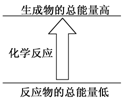

| A. | 镁片与盐酸的反应 | B. | Ba(OH)2•8H2O与NH4Cl晶体的反应 | ||
| C. | 酸碱中和反应 | D. | 乙醇在氧气中的燃烧反应 |
18.洪涝地区欲将河水转化为可饮用水,下列处理过程中较合理的顺序是( )
①化学沉降(加明矾);②消毒杀菌(用漂白粉);③自然沉降;④加热煮沸.
①化学沉降(加明矾);②消毒杀菌(用漂白粉);③自然沉降;④加热煮沸.
| A. | ②①④③ | B. | ③②①④ | C. | ③①②④ | D. | ③①④② |
8.下列热化学方程式中△H的数值表示可燃物燃烧热的是( )
| A. | H2(g)+Cl2(g)═2HCl(g)△H=-184.6 kJ/mol | |
| B. | CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-802.3 kJ/mol | |
| C. | 2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ/mol | |
| D. | C(s)+O2(g)═CO2(g)△H=-285.5 kJ/mol |
15.不慎将油滴在衣服上,要除去油滴的方法通常为( )
| A. | 分液 | B. | 蒸馏 | C. | 过滤 | D. | 溶解 |
12.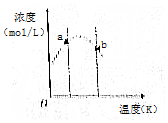 对反应3A(g)+xB(g)?2C(g),将3 molA和2 mol B气体通入体积固定为2L的密闭容器中,测得A与B的转化率相等,C的浓度与温度关系如图所示.下列说法正确的是( )
对反应3A(g)+xB(g)?2C(g),将3 molA和2 mol B气体通入体积固定为2L的密闭容器中,测得A与B的转化率相等,C的浓度与温度关系如图所示.下列说法正确的是( )
 对反应3A(g)+xB(g)?2C(g),将3 molA和2 mol B气体通入体积固定为2L的密闭容器中,测得A与B的转化率相等,C的浓度与温度关系如图所示.下列说法正确的是( )
对反应3A(g)+xB(g)?2C(g),将3 molA和2 mol B气体通入体积固定为2L的密闭容器中,测得A与B的转化率相等,C的浓度与温度关系如图所示.下列说法正确的是( )| A. | 该反应的正反应是吸热反应 | B. | a处反应速率比b处反应速率大 | ||
| C. | 反应方程式中计量数x=1 | D. | b状态时:v(正)=v(逆) |