题目内容
19.现有CH4、C2H4、C2H2、C4H6四种烃①当它们的物质的量相等时,完全燃烧消耗氧气的量最多的是C4H6,生成二氧化碳最少的是CH4,生成水量最少的是C2H2.
②当它们的质量相等时,完全燃烧消耗氧气量最少的是C2H2,生成二氧化碳量最少的是CH4,生成水量最多的是CH4.
分析 ①根据烃燃烧的通式CnHm+(n+$\frac{m}{4}$)O2→nCO2+$\frac{m}{2}$H2O可知,在体积相等的条件下(n+$\frac{m}{4}$)越大,消耗的氧气越多;相同物质的量,分子组成中碳原子越多生成二氧化碳越多,氢原子数越多生成水越多;
②质量相等的条件下,氢原子消耗的氧气大于碳原子消耗的氧气,因此烃分子中,氢元素的含量越多,消耗的氧气就越多,在最简式CHn中,n越大,含氢量越高;分子中含碳量越高,在质量相等时生成的CO2越多,分子组成中含氢量越高,在质量相等的条件下,生成的水最多.
解答 ①根据烃燃烧的通式CnHm+(n+$\frac{m}{4}$)O2→nCO2+$\frac{m}{2}$H2O可知,在体积相等的条件下(n+$\frac{m}{4}$)越大,消耗的氧气越多,所以消耗氧气的量最多的是C4H6;相同物质的量,分子组成中碳原子越多生成二氧化碳越多,氢原子数越多生成水越多,所以生成CO2最少的是CH4,生成H2O最少的是C2H2,
故答案为:C4H6;CH4;C2H2;
②由于在质量相等的条件下,氢原子消耗的氧气大于碳原子消耗的氧气,因此烃分子中,氢元素的含量越多,消耗的氧气就越多,所以消耗氧气的量最少的是C2H2;分子中含碳量越高,在质量相等时生成的CO2越多,所以生成CO2最少的是CH4;分子组成中含氢量越高,在质量相等的条件下,生成的水最多的是CH4.
故答案为:C2H2;CH4;CH4.
点评 本题考查有机物燃烧的有关计算,根据阿伏加德罗定律的度应用,在相同条件下,是物质的量相同还是质量相同,注意审题.

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案
相关题目
9.下列反应属于放热反应的是( )
| A. | 氢气还原氧化铜 | |
| B. | 氢气在氧气中燃烧 | |
| C. | Ba(OH)2•8H2O与NH4Cl反应 | |
| D. | 碳酸钙高温分解成氧化钙和二氧化碳 |
10.下列有机物的命名正确的是( )
| A. | 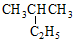 2-乙基丙烷 2-乙基丙烷 | B. | 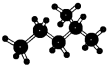 异戊烷 异戊烷 | ||
| C. | 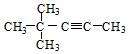 4,4-二甲基-2-戊炔 4,4-二甲基-2-戊炔 | D. | 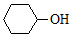 环己酚 环己酚 |
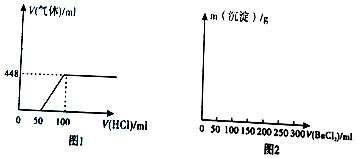
7.已知还原性:I->Br->Cl-,某溶液中含有大量的Cl-、Br-、I-、若向1L该混合溶液中通入一定量的Cl2,溶液中Cl-、Br-、I-的物质的量与通入Cl2的体积(标准状况)的关系如表所示,分析后回答下列问题.
(1)当通入Cl2的体积为2.8L时,溶液中发生反应的离子方程式为Cl2+2I-=I2+2Cl-
(2)原溶液中Cl-、Br-、I-的物质的量浓度之比为10:15:4.
| Cl2的体积(标准状况) | 2.8L | 5.6L | 11.2L |
| n(Cl-) | 1.25mol | 1.5mol | 2mol |
| n(Br-) | 1.5mol | 1.4mol | 0.9mol |
| n(l-) | amol | 0mol | 0mol |
(2)原溶液中Cl-、Br-、I-的物质的量浓度之比为10:15:4.
14.下列反应符合图示的是( )
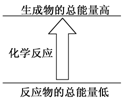

| A. | 镁片与盐酸的反应 | B. | Ba(OH)2•8H2O与NH4Cl晶体的反应 | ||
| C. | 酸碱中和反应 | D. | 乙醇在氧气中的燃烧反应 |
4.下列化学用语正确的是( )
| A. | 某烷烃的命名为:2-甲基-3-乙基丁烷 | |
| B. | 羟基的电子式为: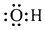 | |
| C. | 丙烷分子的球棍模型: | |
| D. | 丙酸的键线式: |
8.下列热化学方程式中△H的数值表示可燃物燃烧热的是( )
| A. | H2(g)+Cl2(g)═2HCl(g)△H=-184.6 kJ/mol | |
| B. | CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-802.3 kJ/mol | |
| C. | 2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ/mol | |
| D. | C(s)+O2(g)═CO2(g)△H=-285.5 kJ/mol |
9.化学与生产、生活密切相关.下列应用与盐类水解无关的是( )
| A. | 常用热的纯碱溶液清洗餐具上的油污 | |
| B. | “84”消毒液能漂白有色物质 | |
| C. | 常用消石灰改良酸性土壤 | |
| D. | 明矾、硫酸铁常用于净水 |