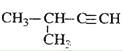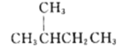题目内容
【题目】设NA为阿伏加德罗常数的值,下列叙述正确的是
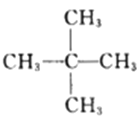
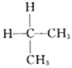
A.标准状况下,22.4L己烷中含有碳原子的数目为6NA
B.常温常压下,7.0g乙烯与丙烯的混合物中含有氢原子的数目为NA
C.50mL18.4mol/L浓硫酸与足量铜微热反应,生成SO2分子数目为0.46NA
D.某密闭容器盛有0.1molN2和0.3molH2,在一定条件下充分反应,转移电子的数目为0.6NA
【答案】B
【解析】
A.标准状况下,22.4L己烷是液体,不能用标况下气体摩尔体积进行物质的量的计算,则含有碳原子的数目不为6NA,故A错误;
B.乙烯和丙烯的最简式为CH2,7.0g混合气体含有0.5mol最简式,含有1mol氢原子,含有氢原子的数目为NA,故B正确;
C.50mL18.4mol/L浓硫酸中含有0.92mol硫酸,Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O浓硫酸完全反应生成0.46mol二氧化硫,由于铜足量,浓硫酸反应后变成稀硫酸,稀硫酸与铜不反应,故生成SO2分子的数目小于0.46NA,故C错误;
CuSO4+SO2↑+2H2O浓硫酸完全反应生成0.46mol二氧化硫,由于铜足量,浓硫酸反应后变成稀硫酸,稀硫酸与铜不反应,故生成SO2分子的数目小于0.46NA,故C错误;
D.由于氮气与氢气生成氨气的反应是可逆反应,0.1molN2和0.3molH2不可能完全转化成0.2mol氨气,因此转移电子的数目小于0.6NA,故D错误;
答案选B。

【题目】探究草酸(H2C2O4)性质,进行如下实验。(已知:室温下,0.1 mol·L1 H2C2O4的pH=1.3)
实验 | 装置 | 试剂a | 现象 |
① |
| Ca(OH)2溶液(含酚酞) | 溶液褪色,产生白色沉淀 |
② | 少量NaHCO3溶液 | 产生气泡 | |
③ | 酸性KMnO4溶液 | 紫色溶液褪色 | |
④ | C2H5OH和浓硫酸 | 加热后产生有香味物质 |
由上述实验所得草酸性质所对应的方程式不正确的是
A. H2C2O4有酸性,Ca(OH)2+ H2C2O4![]() CaC2O4↓+2H2O
CaC2O4↓+2H2O
B. 酸性:H2C2O4> H2CO3,NaHCO3+ H2C2O4![]() NaHC2O4+CO2↑+H2O
NaHC2O4+CO2↑+H2O
C. H2C2O4具有还原性,2![]() +5
+5![]() +16H+
+16H+![]() 2Mn2++10CO2↑+ 8H2O
2Mn2++10CO2↑+ 8H2O
D. H2C2O4可发生酯化反应,HOOCCOOH+2C2H5OH![]() C2H5OOCCOOC2H5+2H2O
C2H5OOCCOOC2H5+2H2O