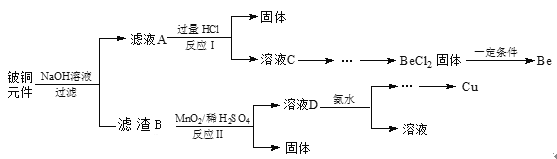
题目内容
【题目】氨和硝酸都是重要的工业原料。
(1)工业上常用过量氨水吸收二氧化硫,该反应的化学方程式为____。
(2)氨氧化法是工业生产中合成硝酸的主要途径。合成的第一步是将氨和空气的混合气通过灼热的铂铑合金网,在合金网的催化下,氨被氧化成一氧化氮,该反应的化学方程式为____。
下列反应中的氨与氨氧化法中的氨作用相同的是___。
A.2Na+2NH3=2NaNH2+H2↑ B.2NH3+3CuO=3Cu+N2+3H2O
C.4NH3+6NO=5N2+6H2O D.HNO3+NH3=NH4NO3
工业中的尾气(假设只有NO和NO2)用烧碱进行吸收,反应的离子方程式为2NO2+2OH﹣=NO2-+NO3-+H2O和NO+NO2+2OH﹣=___+H2O(配平该方程式)。
(3)向27.2gCu和Cu2O的混合物中加入某浓度的稀HNO3500mL,反应过程中产生的气体只有NO。固体完全溶解后,在所得溶液(金属阳离子只有Cu2+)中加入1L1mol·L-1的NaOH溶液使金属离子恰好完全沉淀,此时溶液呈中性,所得沉淀质量为39.2g。
①Cu与稀HNO3反应的离子方程式为________。
②Cu与Cu2O 的物质的量之比为________。
【答案】SO2+2NH3H2O=(NH4)2SO3+H2O[或SO2+2NH3+H2O=(NH4)2SO3] 4NH3+5O2![]() 4NO+6H2O BC 2NO2- 3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O 2∶1
4NO+6H2O BC 2NO2- 3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O 2∶1
【解析】
(1)二氧化硫与氨气反应生成亚硫酸铵;
(2)氨催化氧化生成一氧化氮和水,反应中氨气是还原剂;根据质量守恒和得失电子守恒配平;
(3)①Cu与稀HNO3反应生成硝酸铜、一氧化氮和水,据此书写反应的离子反应方程式;②根据氢氧化钠计算出生成的氢氧化铜的物质的量,再根据铜元素守恒列式计算。
(1)二氧化硫与过量氨气反应生成亚硫酸铵,反应的化学方程式为:SO2+2NH3H2O=(NH4)2SO3+H2O[或SO2+2NH3+H2O=(NH4)2SO3],故答案为:SO2+2NH3H2O=(NH4)2SO3+H2O[或SO2+2NH3+H2O=(NH4)2SO3];
(2)氨催化氧化生成一氧化氮和水,反应方程式为:4NH3+5O2 ![]() 4NO+6H2O,反应中氨气是还原剂,显示氨气的还原性。
4NO+6H2O,反应中氨气是还原剂,显示氨气的还原性。
A.反应2Na+2NH3=2NaNH2+H2↑中,氨气是氧化剂,故A不选;B.反应2NH3+3CuO=3Cu+N2+3H2O中,氨气是还原剂,故B选;C.反应4NH3+6NO=5N2+6H2O中,氨气是还原剂,故C选;D.反应HNO3+NH3=NH4NO3是非氧化还原反应,故D不选;与4NH3+5O2 ![]() 4NO+6H2O中的氨作用相同的是BC;由质量守恒和得失电子守恒,配平为:NO+NO2+2OH-=2NO2-+H2O,故答案为:4NH3+5O2
4NO+6H2O中的氨作用相同的是BC;由质量守恒和得失电子守恒,配平为:NO+NO2+2OH-=2NO2-+H2O,故答案为:4NH3+5O2 ![]() 4NO+6H2O;BC;2NO2-;
4NO+6H2O;BC;2NO2-;
(3)①Cu与稀HNO3反应生成硝酸铜、一氧化氮和水,离子反应方程式为:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,故答案为:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O;
②所得溶液中加入1.0mol/L 的NaOH溶液1.0L,此时溶液呈中性,金属离子已完全沉淀,溶液中溶质为NaNO3,n(NaNO3)=n(NaOH)=1.0mol/L×1.0L=1mol,沉淀为Cu(OH)2,质量为39.2g,物质的量为![]() =0.4mol,根据铜元素守恒有n(Cu)+2n(Cu2O)=n[Cu(OH)2],所以反应后的溶液中n[[Cu(NO3)2]=n[Cu(OH)2]=0.4mol,设Cu、Cu2O的物质的量分别为x、y,则64x+144y=27.2,x+2y=0.4,解得x=0.2,y=0.1,所以Cu与Cu2O 的物质的量之比为2∶1,故答案为:2∶1。
=0.4mol,根据铜元素守恒有n(Cu)+2n(Cu2O)=n[Cu(OH)2],所以反应后的溶液中n[[Cu(NO3)2]=n[Cu(OH)2]=0.4mol,设Cu、Cu2O的物质的量分别为x、y,则64x+144y=27.2,x+2y=0.4,解得x=0.2,y=0.1,所以Cu与Cu2O 的物质的量之比为2∶1,故答案为:2∶1。

 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案【题目】硼(B)可形成H3BO3、NaBH4、NaBO2等化合物,用途广泛。
(1)H3BO3为一元弱酸,常温下,在水中存在如下电离平衡:
H3BO3 + H2O![]() [B(OH)4]-+H+,Ka=5.72×10-10。
[B(OH)4]-+H+,Ka=5.72×10-10。
① 25℃时,0.175 mol/L的H3BO3溶液pH约为_________(取整数)。
② 已知碳酸H2CO3的电离平衡常数为Ka1 = 4.4×10-7,Ka2 = 5.6×10-11。将少量碳酸钠溶液滴加到饱和硼酸溶液中,反应的离子方程式为_________。
(2)在容积恒定为2 L的密闭容器中加入足量BPO4和Na固体并充入一定量的H2(g)发生储氢反应:BPO4(s)+4Na(s)+2H2(g)![]() Na3PO4(s)+NaBH4(s) △H<0
Na3PO4(s)+NaBH4(s) △H<0
① 体系中H2的物质的量与反应时间的关系如表所示:
t /min | 0 | 2 | 4 | 6 | 8 | 10 |
n(H2)/mol | 2.0 | 1.5 | 1.2 | 0.9 | 0.8 | 0.8 |
下列有关叙述正确的是(填标号)_________。
a. 当容器内气体的摩尔质量不再变化时,反应达到平衡状态
b. 10 min时向容器内通入少量H2,则重新达平衡前ν(放氢)> ν(吸氢)
c. 保持温度不变,平衡后再充入1 mol H2,达新平衡时H2的浓度为0.4 mol/L
d. 升高温度,放氢速率加快,重新达到平衡时容器压强增大
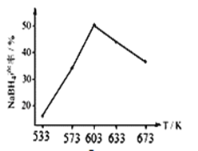
② 下图为相同时间,NaBH4的产率与反应温度的关系曲线。NaBH4的产率在603K之前随温度升高而增大的原因是_________。
(3)NaBH4(s)遇H2O(l)剧烈水解,生成氢气和NaBO2(s)。
① 通常状况下,实验测得3.8gNaBH4(s)发生水解反应放出21.6 kJ热量,写出该反应的热化学方程式_________。
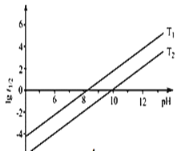
② t1/2为NaBH4水解的半衰期(水解一半所需要的时间,单位为min)。lg t1/2随pH和温度的变化如图所示。溶液pH=4时,NaBH4________(填“能”或“不能”)稳定存在;T1_________T2。(填 “>”或“<”)