题目内容
8.下列指定反应的离子方程式正确的是( )| A. | 氯气溶于水:Cl2+H2O═2H++Cl-+ClO- | |
| B. | NaHCO3溶液中加足量Ba(OH)2溶液:HCO3-+Ba2++OH-═BaCO3↓+H2O | |
| C. | 酸性溶液中KIO3与KI反应生成I2:IO3-+I-+6H+═I2+3H2O | |
| D. | Na2CO3溶液中CO32-的水解:CO32-+H2O═HCO3-+OH- |
分析 A.次氯酸为弱酸,应保留化学式;
B.氢氧化钡过量反应生成碳酸钡沉淀、氢氧化钠和水;
C.电荷不守恒;
D.碳酸根离子部分水解生成碳酸氢根离子和氢氧根离子,为可逆反应.
解答 解:A.氯气溶于水,离子方程式:Cl2+H2O═H++Cl-+HClO,故A错误;
B.NaHCO3溶液中加足量Ba(OH)2溶液,离子方程式:HCO3-+Ba2++OH-═BaCO3↓+H2O,故B正确;
C.酸性溶液中KIO3与KI反应生成I2,离子方程式:IO3-+5I-+6H+═3I2+3H2O,故C错误;
D.Na2CO3溶液中CO32-的水解,离子方程式:CO32-+H2O═HCO3-+OH-,故D错误;
故选:B.
点评 本题考查了离子方程式的书写,明确反应实质及离子方程式书写方法是解题关键,注意盐类水解规律,题目难度不大.

练习册系列答案
相关题目
18.中学化学很多“规律”都有其适用范围,下列根据有关“规律”推出的结论合理的是( )
| A. | 根据弱酸越稀越电离的规律,0.2mol•L-1 CH3COOH的pH值比0.1mol•L-1 CH3COOH的 pH值大 | |
| B. | 根据主族元素最高正化合价与族序数的关系,推出卤族元素最高正价都是+7 | |
| C. | 根据溶液的pH与溶液酸碱性的关系,推出pH=6.8的溶液一定显酸性 | |
| D. | 根据较强酸可以制取较弱酸的规律,推出CO2通入NaClO溶液中能生成HClO |
19.某同学探究氨和铵盐的性质,相关实验操作及现象描述正确的是( )
| A. | 室温下测定等浓度氨水和NaOH溶液的pH,比较氨水和NaOH碱性强弱 | |
| B. | 将氨水缓慢滴入AlCl3溶液中,研究Al(OH)3的两性 | |
| C. | 将蘸有浓氨水和浓硫酸的玻璃棒靠近,观察到白烟 | |
| D. | 加热除去NH4Cl中的少量NaHC03 |
16.日常饮用水中NO3-的含量是水质卫生检验的重要标准之一,达到一定浓度时会对人体健康产生危害.为了降低饮水中NO3-的浓度,某自来水厂设计了如下方案:
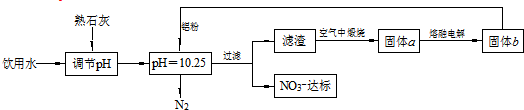
下列说法不正确的是( )

下列说法不正确的是( )
| A. | 该方案在调节pH时,若pH过大或过小都会造成Al的利用率降低 | |
| B. | 为了降低能耗,工业上往往用AlCl3代替固体a来制备固体b | |
| C. | 用熟石灰调节PH主要原因是价格便宜且引入的Ca2+对人体无害 | |
| D. | 在加入铝粉的反应中,氧化产物和还原产物的物质的量之比为10:3 |
13.下列溶液中微粒浓度关系一定正确的是( )
| A. | 0.1mol/L的硫酸铵溶液中:c(NH4+)>c(SO42-)>c(H+) | |
| B. | 室温下,pH=7的醋酸和醋酸钠的混合溶液中:c(CH3COO-)>c(Na+) | |
| C. | 将水加热到100℃,pH=6:c(H+)>c(OH-) | |
| D. | 同浓度的三种溶液:①CH3COONH4 ②NH4Cl ③NH3•H2O中,c(NH4+)由大到小的顺序是②③① |

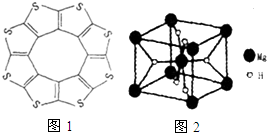 氢能被视为21世纪最具发展潜力的清洁能源.
氢能被视为21世纪最具发展潜力的清洁能源.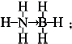 ;与氨硼烷互为等电子体的有机小分子是CH3CH3(写结构简式).
;与氨硼烷互为等电子体的有机小分子是CH3CH3(写结构简式).