题目内容
现有25℃的下列物质:
①0.1mol?L-1的Na2CO3溶液,②0.1mol?L-1的NaHCO3溶液,③0.1mol?L-1氨水,④pH=1的盐酸,⑤pH=1的醋酸,⑥pH=4的NH4Cl溶液
回答下列问题
(1)溶液中的溶质会发生水解反应的是 (用序号表示,下同),溶液中的溶质存在电离平衡的是
(2)①②中pH较大的是 ,④⑤中溶质的物质的量浓度较大的是
(3)⑤中c(OH-)是 mol?L-1,⑥中由水电离产生的c(H+)是 mol?L-1
(4)现有Vml③,用④来滴定,当消耗④的体积 Vml(填“<”,“>”或“﹦”)时,水的电离程度最大,理由是 ,此时溶液中各离子的浓度关系是 .
①0.1mol?L-1的Na2CO3溶液,②0.1mol?L-1的NaHCO3溶液,③0.1mol?L-1氨水,④pH=1的盐酸,⑤pH=1的醋酸,⑥pH=4的NH4Cl溶液
回答下列问题
(1)溶液中的溶质会发生水解反应的是
(2)①②中pH较大的是
(3)⑤中c(OH-)是
(4)现有Vml③,用④来滴定,当消耗④的体积
考点:盐类水解的应用
专题:盐类的水解专题
分析:(1)溶液中的溶质会发生水解的是有弱离子的盐,溶液中的溶质存在电离平衡是弱酸阴离子、弱电解质;
(2)同浓度碳酸钠溶液和碳酸氢钠溶液中碳酸根离子水解程度大于碳酸氢根离子;盐酸是强酸,醋酸是弱酸存在电离平衡;
(3)依据溶液中离子积常数计算;
(4)盐酸滴定一水合氨溶液恰好反应生成强酸弱碱盐,盐溶液中铵根离子水解促进水的电离,酸或碱抑制水的电离.
(2)同浓度碳酸钠溶液和碳酸氢钠溶液中碳酸根离子水解程度大于碳酸氢根离子;盐酸是强酸,醋酸是弱酸存在电离平衡;
(3)依据溶液中离子积常数计算;
(4)盐酸滴定一水合氨溶液恰好反应生成强酸弱碱盐,盐溶液中铵根离子水解促进水的电离,酸或碱抑制水的电离.
解答:
解:(1)溶液中的溶质会发生水解的是有弱离子的盐,①0.1mol?L-1的Na2CO3溶液中碳酸根离子水解,②0.1mol?L-1的NaHCO3溶液中碳酸氢根离子水解,⑥pH=4的NH4Cl溶液中铵根离子水解,溶液中的溶质存在电离平衡是弱酸阴离子、弱电解质,②0.1mol?L-1的NaHCO3溶液碳酸氢根离子存在电离平衡,③0.1mol?L-1氨水溶液中存在一水合氨电离平衡,⑤pH=1的醋酸溶液中存在醋酸电离平衡;
故答案为:①②⑥;②③⑤;
(2)同浓度碳酸钠溶液和碳酸氢钠溶液中碳酸根离子水解程度大于碳酸氢根离子,溶液PH①;盐酸是强酸,醋酸是弱酸存在电离平衡,相同PH的盐酸溶液和醋酸溶液中溶质浓度醋酸大,溶质的物质的量浓度较大的是⑤;
故答案为:①;⑤;
(3)依据溶液中离子积常数计算,pH=1的醋酸溶液中氢氧根离子浓度c(OH-)=
=10-13mol/L,⑥pH=4的NH4Cl溶液中由水电离产生的C(H+)=10-4mol/L;
故答案为:10-13;10-4;
(4)现有Vml③0.1mol?L-1氨水,用④pH=1的盐酸来滴定,当消耗④的体积=Vml,盐酸滴定一水合氨溶液恰好反应生成强酸弱碱盐,盐溶液中铵根离子水解促进水的电离,水的电离程度最大,酸或碱抑制水的电离,氯化铵溶液中铵根离子水解显酸性,离子浓度大小为:c(Cl-)>c(NH4+)>c(H+)>c(OH-);
故答案为:=;两溶液恰好反应生成氯化铵,铵根离子水解促进水的电离,而在酸或碱过量时都会抑制水的电离;c(Cl-)>c(NH4+)>c(H+)>c(OH-).
故答案为:①②⑥;②③⑤;
(2)同浓度碳酸钠溶液和碳酸氢钠溶液中碳酸根离子水解程度大于碳酸氢根离子,溶液PH①;盐酸是强酸,醋酸是弱酸存在电离平衡,相同PH的盐酸溶液和醋酸溶液中溶质浓度醋酸大,溶质的物质的量浓度较大的是⑤;
故答案为:①;⑤;
(3)依据溶液中离子积常数计算,pH=1的醋酸溶液中氢氧根离子浓度c(OH-)=
| 10-14 |
| 0.1 |
故答案为:10-13;10-4;
(4)现有Vml③0.1mol?L-1氨水,用④pH=1的盐酸来滴定,当消耗④的体积=Vml,盐酸滴定一水合氨溶液恰好反应生成强酸弱碱盐,盐溶液中铵根离子水解促进水的电离,水的电离程度最大,酸或碱抑制水的电离,氯化铵溶液中铵根离子水解显酸性,离子浓度大小为:c(Cl-)>c(NH4+)>c(H+)>c(OH-);
故答案为:=;两溶液恰好反应生成氯化铵,铵根离子水解促进水的电离,而在酸或碱过量时都会抑制水的电离;c(Cl-)>c(NH4+)>c(H+)>c(OH-).
点评:本题考查了盐类水解的分析应用,酸碱反应后溶液酸碱性的分析判断,离子积常数,离子浓度大小比较是解题关键,题目难度中等.

练习册系列答案
相关题目
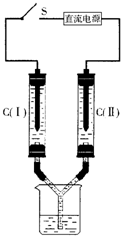 如图所示装置,两玻璃管中盛满滴有酚酞溶液的NaCl饱和溶液,C(Ⅰ)、C(Ⅱ)为多孔石墨电极.接通S后,C(Ⅱ)附近溶液变红,两玻璃管中有气体生成.下列说法正确的是( )
如图所示装置,两玻璃管中盛满滴有酚酞溶液的NaCl饱和溶液,C(Ⅰ)、C(Ⅱ)为多孔石墨电极.接通S后,C(Ⅱ)附近溶液变红,两玻璃管中有气体生成.下列说法正确的是( )| A、C(Ⅰ)电极产生可燃性气体 | ||||
| B、C(Ⅱ)的电极附近溶液呈碱性 | ||||
| C、C(Ⅱ) 电极产生的气体可使湿润的碘化钾淀粉试纸变蓝色 | ||||
D、电解过程中发生的化学方程式为:2NaCl
|