题目内容
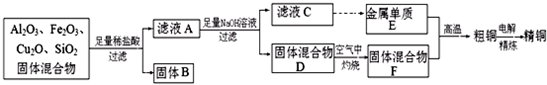
某化学兴趣小组利用由Cu2O、Al2O3、Fe2O3、SiO2组成的混合物,模拟工业上提取铜的工艺,设计如图所示的简单操作流程:
提示:Cu+在酸性条件下不稳定,易生成金属Cu和Cu2+.
(1)若固体B的成分为混合物,则其成分的化学式为 .此时,滤液A中铁元素的存在形式为 (填写离子符号).
(2)金属E与固体F发生反应的化学方程式为: .
(3)检验粗铜中含有金属E单质的试剂是 ,反应的离子方程式为 .
(4)用电解法将上述粗铜进行精炼时,下列叙述正确的是 .
A.电解时以精铜作阴极
B.电解时阴极发生氧化反应
C.粗铜连接电源负极,其电极反应是Cu-2e-=Cu2+
D.电解后,电解液中Cu2+浓度减小.

提示:Cu+在酸性条件下不稳定,易生成金属Cu和Cu2+.
(1)若固体B的成分为混合物,则其成分的化学式为
(2)金属E与固体F发生反应的化学方程式为:
(3)检验粗铜中含有金属E单质的试剂是
(4)用电解法将上述粗铜进行精炼时,下列叙述正确的是
A.电解时以精铜作阴极
B.电解时阴极发生氧化反应
C.粗铜连接电源负极,其电极反应是Cu-2e-=Cu2+
D.电解后,电解液中Cu2+浓度减小.
考点:物质分离和提纯的方法和基本操作综合应用
专题:实验设计题
分析:Cu2O与盐酸反应生成Cu和Cu2+,SiO2与盐酸不反应,Fe2O3与盐酸反应生成Fe3+,与Cu反应生成Fe2+,固体B为SiO2和Cu,滤液A中含有Cu2+、Fe2+、Al3+,加入足量的NaOH溶液,滤液C中含有AlO2-,金属E为Al,固体D为Cu(OH)2和Fe(OH)3的混合物,在空气中灼烧,F为CuO和Fe2O3的混合物,粗铜为Cu、Al和Fe的混合物,经过电解可的纯铜,以此解答该题.
解答:
解:Cu2O与盐酸反应生成Cu和Cu2+,SiO2与盐酸不反应,Fe2O3与盐酸反应生成Fe3+,与Cu反应生成Fe2+,固体B为SiO2和Cu,滤液A中含有Cu2+、Fe2+、Al3+,加入足量的NaOH溶液,滤液C中含有AlO2-,金属E为Al,固体D为Cu(OH)2和Fe(OH)3的混合物,在空气中灼烧,F为CuO和Fe2O3的混合物,粗铜为Cu、Al和Fe的混合物,经过电解可的纯铜,
(1)由以上分析可知固体B的成分为SiO2和Cu,滤液A中铁元素的存在形式为Fe2+,
故答案为:SiO2和Cu;Fe2+;
(2)E为Al,F为CuO和Fe2O3的混合物,反应的相关方程式为2Al+Fe2O3
Al2O3+2Fe、2Al+3CuO
Al2O3+3Cu,
故答案为:2Al+Fe2O3
Al2O3+2Fe、2Al+3CuO
Al2O3+3Cu;
(3)可用NaOH溶液检验检验粗铜中含有金属Al,发生2Al+2OH-+2H2O=2AlO2-+3H2↑,
故答案为:NaOH溶液;2Al+2OH-+2H2O=2AlO2-+3H2↑;
(4)A.电解时以粗铜作阳极,纯铜为阴极,故A正确;
B.电解时阴极发生还原反应,阳极发生氧化反应,故B错误;
C.粗铜连接电源正极,纯铜连接电源负极,其电极反应是Cu2++2e-═Cu,故C错误;
D.电解后,由于阳极为粗铜,溶液中含有Fe2+、Al3+,而阴极只生成Cu,则电解液中Cu2+浓度减小,故D正确.
故答案为:AD.
(1)由以上分析可知固体B的成分为SiO2和Cu,滤液A中铁元素的存在形式为Fe2+,
故答案为:SiO2和Cu;Fe2+;
(2)E为Al,F为CuO和Fe2O3的混合物,反应的相关方程式为2Al+Fe2O3
| ||
| ||
故答案为:2Al+Fe2O3
| ||
| ||
(3)可用NaOH溶液检验检验粗铜中含有金属Al,发生2Al+2OH-+2H2O=2AlO2-+3H2↑,
故答案为:NaOH溶液;2Al+2OH-+2H2O=2AlO2-+3H2↑;
(4)A.电解时以粗铜作阳极,纯铜为阴极,故A正确;
B.电解时阴极发生还原反应,阳极发生氧化反应,故B错误;
C.粗铜连接电源正极,纯铜连接电源负极,其电极反应是Cu2++2e-═Cu,故C错误;
D.电解后,由于阳极为粗铜,溶液中含有Fe2+、Al3+,而阴极只生成Cu,则电解液中Cu2+浓度减小,故D正确.
故答案为:AD.
点评:本题考查考查物质的制备以及分离和提纯等知识,侧重于考查学生综合运用化学知识的能力,为高考常见题型,难度中等.

练习册系列答案
相关题目
下列关于气体摩尔体积的几种说法错误的是( )
| A、22.4L二氧化碳的物质的量为1mol |
| B、标准状况下,1mol H2O的体积为22.4L |
| C、0.1mol H2、0.2mol O2、0.3mol N2和0.4mol CO2组成的混合气体在标准状况下的体积约为22.4L |
| D、在同温同压下,相同体积的任何气体所含分子数相同 |