题目内容
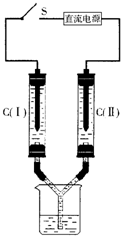 如图所示装置,两玻璃管中盛满滴有酚酞溶液的NaCl饱和溶液,C(Ⅰ)、C(Ⅱ)为多孔石墨电极.接通S后,C(Ⅱ)附近溶液变红,两玻璃管中有气体生成.下列说法正确的是( )
如图所示装置,两玻璃管中盛满滴有酚酞溶液的NaCl饱和溶液,C(Ⅰ)、C(Ⅱ)为多孔石墨电极.接通S后,C(Ⅱ)附近溶液变红,两玻璃管中有气体生成.下列说法正确的是( )| A、C(Ⅰ)电极产生可燃性气体 | ||||
| B、C(Ⅱ)的电极附近溶液呈碱性 | ||||
| C、C(Ⅱ) 电极产生的气体可使湿润的碘化钾淀粉试纸变蓝色 | ||||
D、电解过程中发生的化学方程式为:2NaCl
|
考点:原电池和电解池的工作原理
专题:电化学专题
分析:电解NaCl溶液时,阳极是氯离子放电生成氯气,阴极是水电离出的氢离子放电生成氢气,导致氢氧根离子的浓度增大,使阴极显碱性,据此解答.
解答:
解:电解NaCl溶液时,阳极是氯离子放电生成氯气,阴极是水电离出的氢离子放电生成氢气,导致氢氧根离子的浓度增大,使阴极显碱性,C(Ⅱ)附近溶液变红,应为电解池的阴极,
A、C(Ⅰ)电极是阳极,生成氯气无可燃性,故A错误;
B、C(Ⅱ)电极附近溶液变红,显碱性是阴极,故B正确;
C、C(Ⅱ)电极附近溶液变红,显碱性是阴极,生成氢气,不能使淀粉碘化钾试纸变色,故C错误;
D、电解NaCl的水溶液不生成Na,故D错误;
故选B.
A、C(Ⅰ)电极是阳极,生成氯气无可燃性,故A错误;
B、C(Ⅱ)电极附近溶液变红,显碱性是阴极,故B正确;
C、C(Ⅱ)电极附近溶液变红,显碱性是阴极,生成氢气,不能使淀粉碘化钾试纸变色,故C错误;
D、电解NaCl的水溶液不生成Na,故D错误;
故选B.
点评:本题考查了电解NaCl的水溶液的两极产物及产物判断,关键是阴极显碱性,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
工业生产上常使用催化剂,因为它可以( )
| A、提高反应进行的程度 |
| B、使平衡向正反应方向移动 |
| C、是生成物更纯净 |
| D、使容器中气体的密度不再发生变化 |
下列离子方程式正确的是( )
| A、大理石溶于稀盐酸中:2H++CO3 2-=H2O+CO2↑ |
| B、铝离子与过量氨水反应:Al3++4NH3?H2O=AlO2-+2H2O+4NH4+ |
| C、二氧化硅与氢氧化钠溶液反应:SiO2+2OH-=SiO32-+H2O |
| D、硫酸铜与氢氧化钡溶液反应:Ba2++SO42-=BaSO4↓ |
HNO3的酸酐是N2O5,HNO2的酸酐是N2O3,有人认为NO2可以成为HNO3、HNO2的混合酸酐
①2NO2+2NaOH═NaNO3+NaNO2+H2O
②2NO2+H2O═HNO3+HNO2
③NO2+NO+2NaOH═2NaNO2+H2O
三个化学方程式所代表的反应中你认为能说明NO2是混合酸酐的是( )
①2NO2+2NaOH═NaNO3+NaNO2+H2O
②2NO2+H2O═HNO3+HNO2
③NO2+NO+2NaOH═2NaNO2+H2O
三个化学方程式所代表的反应中你认为能说明NO2是混合酸酐的是( )
| A、①②③ | B、②③ | C、①③ | D、①② |
下列关于气体摩尔体积的几种说法错误的是( )
| A、22.4L二氧化碳的物质的量为1mol |
| B、标准状况下,1mol H2O的体积为22.4L |
| C、0.1mol H2、0.2mol O2、0.3mol N2和0.4mol CO2组成的混合气体在标准状况下的体积约为22.4L |
| D、在同温同压下,相同体积的任何气体所含分子数相同 |
下列分离或除杂的方法不正确的是( )
| A、用分液法分离水和酒精 |
| B、用蒸馏法分离苯和溴苯 |
| C、用过滤方法提纯苯甲酸 |
| D、用饱和碳酸氢钠溶液除去二氧化碳中混有的少量氯化氢气体 |