题目内容
14.700℃时,向容积为2L的密闭容器中充入一定量的CO和H2O,发生反应:CO(g)+H2O(g)?CO2(g)+H2(g),反应过程中测定的部分数据见下表(表中t1<t2),下列说法正确的是( )| 反应时间/min | n(CO)/mol | n(H2O)/mol |
| 0 | 1.20 | 0.60 |
| t1 | 0.80 | |
| t2 | 0.20 |
| A. | 反应在t1 min内的平均速率为v(H2)=$\frac{0.40}{{t}_{1}}$mol/(L•min) | |
| B. | 保持其他条件不变,起始时向容器中充入0.60 mol CO和1.20 mol H2,到达平衡时,n(CO2)=0.40 mol | |
| C. | 保持其他条件不变,向平衡体系中再通入0.20 mol CO,与原平衡相比,达到新平衡时CO转化率减小,H2的体积分数也减小 | |
| D. | 温度升至800℃,上述反应平衡常数为0.64,则正反应为吸热反应 |
分析 A、由表中数据可知,t1min内参加反应的CO的物质的量为1.2mol-0.8mol=0.4mol,根据v=$\frac{△c}{△t}$计算v(CO),再根据速率之比等于化学计量数之比计算v(H2);
B、CO与H2O按物质的量比1:1反应,充入0.60 mol CO和1.20 mol H2O与充入1.20 mol CO和0.6mol H2O到达平衡时对应生成物的浓度、物质的量相同;
C、保持其他条件不变,增加一种反应物的浓度,平衡向正反应方向移动,另一种反应物的转化率增大,自身转化率降低;
D、t1min时n(CO)=0.8mol,n(H2O)=0.6mol-0.4mol=0.2mol,t2min时n(H2O)=0.2mol,说明t1min时反应已经达到平衡状态,反应前后气体的体积不变,利用物质的量代替浓度计算700℃时平衡常数,比较不同温度下的平衡常数大小判断反应的热效应.
解答 解:A、由表中数据可知,t1min内参加反应的CO的物质的量为1.2mol-0.8mol=0.4mol,v(CO)=$\frac{0.4mol÷2L}{{t}_{1}}$=$\frac{0.2}{{t}_{1}}$mol/(L•min),速率之比等于化学计量数之比计算v(H2)=v(CO)=$\frac{0.2}{{t}_{1}}$mol/(L•min),故A错误;
B、CO与H2O按物质的量比1:1反应,充入0.60 mol CO和1.20 mol H2O与充入1.20 mol CO和0.6mol H2O,平衡时生成物的浓度对应相同,t1min时n(CO)=0.8mol,n(H2O)=0.6mol-0.4mol=0.2mol,t2min时n(H2O)=0.2mol,说明t1min时反应已经达到平衡状态,根据化学方程式可知,则生成的n(CO2)=0.4mol,故B正确;
C、保持其他条件不变,向平衡体系中再通入0.20molH2O,与原平衡相比,平衡向右移动,达到新平衡时CO转化率增大,H2O转化率减小,H2O的体积分数会增大,故C正确;
D、t1min时n(CO)=0.8mol,n(H2O)=0.6mol-0.4mol=0.2mol,t2min时n(H2O)=0.2mol,说明t1min时反应已经达到平衡状态,此时n(CO)=0.8mol,n(H2O)=0.2mol,n(CO2)=c(H2)=△n(CO)=1.2mol-0.8mol=0.4mol,700℃时平衡常数K=$\frac{(0.4mol÷2L)×(0.4mol÷2L)}{(0.8mol÷2L)×(0.2mol÷2L)}$=1,温度升至800℃,上述反应平衡常数为0.64,说明温度升高,平衡是向左移动,故正反应为放热反应,故D错误;
故选:BC.
点评 本题主要考查化学反应速率计算、化学平衡移动及平衡常数计算与运用,题目难度不大,注意基础的积累.

 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案 N、C、S元素的单质及化合物在工农业生成中有着重要的应用
N、C、S元素的单质及化合物在工农业生成中有着重要的应用Ⅰ.CO与Cl2在催化剂的作用下合成光气(COCl2).某温度下,向2L的密闭容器中投入一定量的CO和Cl2,在催化剂的作用下发生反应:CO(g)+Cl2(g)?COCl2(g)反应过程中测定的部分数据如表:
| t/min | n(CO)/mol | n(Cl2)/mol |
| 0 | 1.20 | 0.60 |
| 1 | 0.90 | |
| 2 | 0.80 | |
| 4 | 0.20 |
(2)图1是T℃时,CO和Cl2的物质的量浓度随时间(t)的变化情况.用COCl2表示2min内的反应速率v(COCl2)=0.1mol/(L.min).该温度下的平衡常数K=5.
(3)在一容积可变的密闭容器中充入10molCO和20molCl2,CO的平衡转化率随温度(T)、压强(P)的变化如图1所示.
①下列说法能判断该反应达到化学平衡的是BD(填字母序号).
A.Cl2的消耗速率等于COCl2的生成速率
B.Cl2的体积分数不变
C.Cl2的转化率和CO的转化率相等
D.混合气体的平均摩尔质量不再改变
②比较A、B两点压强大小:P(A)<P(B)(填“>”、“<”或“=”)
③若达到化学平衡状态A时,容器的体积为20L.如果反应开始时仍充入10molCO和20molCl2,则在平衡状态B时容器的体积为4L.
Ⅱ甲醇是一种重要的化工原料,查资料,甲醇的制取可用以下两种方法:
(1)可用CO和H2制取甲醇:
已知CO、CH3OH和H2的燃烧分别是283kj/mol、726.83kj/mol、285.2kj/mol写出由 CO和H2制取甲醇的热化学方程式CO(g)+2H2(g)=CH3OH(l),△H=-126.57kJ/mol.
(2)用电化学法制取:某模拟植物光合作用的电化学装置如图2,该装置能将H2O和CO2转化为O2和甲醇(CH3OH).
①该装置工作时H+向b区移动(填“a”或“b”)
②b极上的电极反应式为6H++CO2+6e-=CH3OH+H2O.
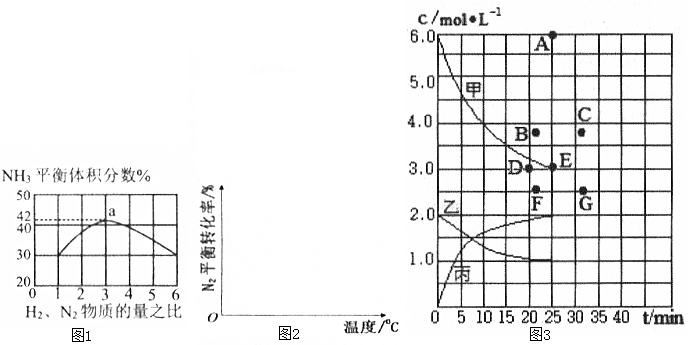
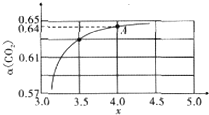
(1)已知:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ•mol-1.如图1表示500℃、60.0MPa条件下,原料气H2和N2的投料比与平衡时NH3体积分数的关系.
①工业上合成氨的温度一般控制在500℃,原因是该温度下催化剂的活性最好.
②根据图1中a点数据计算N2的平衡体积分数为14.5%,此时H2和N2的转化率之比为1:1.
(2)合成氨工业中,在其他条件相同时,请你画出N2的平衡转化率在不同压强(p1>p2)下随温度变化的曲线图.

(3)在500℃,反应N2(g)+3H2(g)?2NH3(g)中,将2mol N2和6mol H2充入一个固定容积为1L的密闭容器中,随着反应的进行,气体混合物中n(H2)、n(NH3)与反应时间t的关系如表所示.
| t/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| N(H2)/mol | 6.00 | 4.50 | 3.60 | 3.30 | 3.03 | 3.00 | 3.00 |
| N(NH3)/mol | 0 | 1.00 | 1.60 | 1.80 | 1.98 | 2.00 | 2.00 |
②该温度下,若向同容积的另一容器中投入的N2、H2、NH3浓度均为3mol/L,此时v正大于v逆(填“大于”、“小于”或“等于”).
③根据上表中数据得到的“浓度-时间”关系可用如图3中曲线表示,其中表示c(N2)-t的曲线是乙(填“甲”、“乙”或“丙”).在此温度下,若起始充入4molN2和12mol H2,反应刚达到平衡时,氢气的浓度可用B点表示(从A~G点中选择).
(4)近年,又有科学家提出在常温、常压、催化剂等条件下合成氨气的新思路,反应原理为:2N2(g)+6H2O(I)?4NH3(g)+3O2(g),则其反应热△H=+1530 kJ•mol-1.(已知:2H2(g)+O2(g)=2H2O(I)△H=-571.6kJ•mol-1)
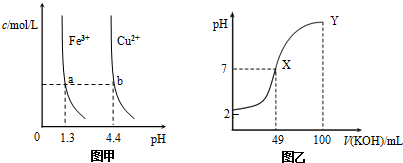
| A. | 由图甲知:Ksp[Fe(OH)3]<Ksp[Cu(OH)2] | |
| B. | 由图甲知:a、b点溶液中Kw,b点的大 | |
| C. | 由图乙知:HA为强酸 | |
| D. | 由图乙知:Y点对应的溶液中c(K+)>c(A-)>c(OH-) |
 | 0 | 2 | 4 | 6 | 8 | 10 |
| c(N2O4) | 0.100 | c1 | 0.050 | c3 | a | b |
| c(NO2) | 0.000 | 0.060 | c2 | 0.120 | 0.120 | 0.120 |
(1)该反应达到平衡时,四氧化二氮的转化率为60%,表中c2>c3、a=b(填“>”、“<”或“=”).
(2)2min时四氧化二氮的浓度c1=0.070mol/L,在0~2min时间段内,四氧化二氮的平均反应速率为0.015mol/(L•min).
(3)100℃时,该反应的平衡常数K=0.36
(4)若在相同情况下最初向该容器充入的是二氧化氮气体,要达到上述同样的平衡状态,二氧化氮的起始浓度是0.200mol/L.
 尿素作为一种中性肥料,适用于各种土壤和植物.它易保存,使用方便,对土壤的破坏作用小,是目前使用量较大的一种化学氮肥.
尿素作为一种中性肥料,适用于各种土壤和植物.它易保存,使用方便,对土壤的破坏作用小,是目前使用量较大的一种化学氮肥.


