题目内容
14.碘元素有“智力元素”之称.研究性学习小组做了如下实验探究海带中碘元素存在并测定其中碘元素的含量.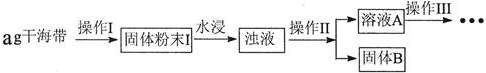
(1)操作Ⅰ为灼烧,则灼烧时用坩埚 盛装海带,操作Ⅱ为过滤
(2)水浸时通常要将悬浊液煮沸2-3min,目的是加快含碘物质在水中的溶解,以使灰烬中的含碘物质尽可能多的进入溶液
(3)操作Ⅲ,是同学们对溶液A中碘元素的存在形式进行的探究实验.
[推测]:①以IO3-形式存在; ②以I-形式存在
[查阅资料]:IO3-具有较强的氧化性,I2+2S2O32-═2I-+S4O62-
将上述溶液稀释配制成200mL溶液,请完成下列实验探究.限选试剂:3%H2O2溶液、KSCN溶液、FeCL2溶液、稀硫酸
| 序号 | 实验方案 | 实验现象 | 结论 |
| ① | 取少量稀释后的溶液A加入淀粉后再用硫酸酸化,分装于试管Ⅰ、Ⅱ | 无现象 |  |
| ② | 往试管Ⅰ中加入FeCl2溶液后,加入2滴KSCN溶液并振荡 | 无现象 | 证明不是以IO3-形式存在 |
| ③ | 往试管Ⅱ中加入3%H2O2溶液并振荡 | 溶液变蓝 | 证明以I-形式存在 |
①取20mL稀释后溶液A分别于锥形瓶,分别用酸式滴定管滴加0.01mol/LKMnO4
溶液至溶液刚显浅红色,将I-氧化为I2并得到溶液B
②在溶液B加入两滴淀粉溶液,用0.01mol/LNaS2O3溶液,滴定至终点,终点现象为溶液蓝色刚好褪去,30s内不恢复蓝色,记录数据,重复上测定步骤①、②两次,三次平均消耗Na2S2O3溶液体积为VmL,计算海带中碘元素的百分含量$\frac{1.27V}{a}$×100%.
(假设操作Ⅰ、Ⅱ过程中碘不损失,原子量I-127)
分析 干海带灼烧得到固体粉末Ⅰ,水浸后得到浊液,操作Ⅱ是过滤得到溶液A,操作Ⅲ是将上述溶液稀释配制成200mL溶液,用高锰酸钾溶液氧化得到碘单质,用硫代硫酸钠吸收碘单质测定碘的含量,
(1)依据流程图分析,操作Ⅰ固体灼烧在坩埚中;操作Ⅱ是分离固体和液体的实验操作过滤;
(2)加热使含碘物质更多地溶解于水溶液中;
(3)②利用亚铁离子具有还原性,碘酸根离子在酸性溶液中具有氧化性,检验是否含有铁离子;
③利用试剂过氧化氢具有氧化性可以氧化碘离子为碘单质,遇到淀粉变蓝;
(4)依据A溶液中碘离子被高锰酸钾溶液氧化为碘单质,碘单质被硫代硫酸钠溶液还原为碘离子,中和滴定过程中,到蓝色恰好褪去不再变化证明反应到终点;依据离子方程式计算得到碘 元素含量.
解答 解:(1)流程图分析,操作Ⅰ固体灼烧在坩埚中;操作Ⅱ是分离固体和液体的实验操作过滤,
故答案为:坩埚;过滤;
(2)水浸要将悬浊液煮沸2-3min是为了增大含碘物质的溶解度,使更多的含碘物质溶解,
故答案为:加快含碘物质在水中的溶解,以使灰烬中的含碘物质尽可能多的进入溶液;
(3)②利用亚铁离子具有还原性,碘酸根离子在酸性溶液中具有氧化性,检验是否含有铁离子,往试管I中加入氯化亚铁溶液,后加入2滴KSCN溶液并振荡,无血红色出现证明不是以IO3-形式存在;
故答案为:FeCl2溶液,后加入2滴KSCN溶液并振荡;
③往试管II中加入3%过氧化氢具有氧化性可以氧化碘离子为碘单质,遇到淀粉变蓝,
故答案为:3% H2O2溶液并振荡;溶液变蓝;
(4)A溶液中碘离子被高锰酸钾溶液氧化为碘单质,碘单质被硫代硫酸钠溶液还原为碘离子,中和滴定过程中,到蓝色恰好褪去不再变化证明反应到终点;设碘离子物质的量为x,
2I-~I2~2Na2S2O3
2 2
x 0.01mol/L×V×10-3L
x=V×10-5mol
200ml溶液中含碘元素物质的量为=V×10-4mol
海带中碘元素的百分含量=$\frac{V×1{0}^{-4}×127g/mol}{ag}$×100%=$\frac{1.27V}{a}$×100%,
故答案为:溶液蓝色刚好褪去,30s内不恢复蓝色,$\frac{1.27V}{a}$×100%.
点评 本题考查了物质制备的流程分析判断,实验方案的设计原则和步骤,滴定实验的计算应用,反应现象和物质性质是解题关键,题目难度中等.

| A. | 需要加热才能发生的反应不一定是吸热反应 | |
| B. | 任何放热反应在常温条件下一定能够发生 | |
| C. | 反应物和生成物具有的总能量决定了反应是吸热还是放热 | |
| D. | 吸热反应在一定条件下(如加热等)也能够发生 |
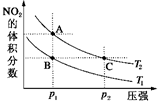 反应N2O4(g)?2NO2(g)△H=+57kJ•mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.正确的是( )
反应N2O4(g)?2NO2(g)△H=+57kJ•mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.正确的是( )| A. | A、C两点的反应速率:A>C | |
| B. | A、C两点气体的颜色:A深,C浅 | |
| C. | A、C两点气体的平均相对分子质量:A>C | |
| D. | 由状态B到状态A,可以用加热的方法 |
| A. | ②③① | B. | ③② | C. | ②①③ | D. | ①②③ |
| A. | 盐酸滴在石灰石上:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| B. | 少量CO2通入NaOH溶液中,:CO2+2OH-═CO32-+H2O | |
| C. | NaOH溶液和KHSO4溶液反应:OH-+H+═H2O | |
| D. | Na2O溶于稀盐酸:O2-+2H+═H2O |




 某种物质的结构如图所示,它是某种烃的衍生物的3个分子间相互加成生成的,这种烃的衍生物是甲醛.
某种物质的结构如图所示,它是某种烃的衍生物的3个分子间相互加成生成的,这种烃的衍生物是甲醛.