题目内容
下列各组物质中,化学键的类型(离子键、共价键)相同的是( )
| A、CO和MgCl2 |
| B、NH4F和NaF |
| C、Na2O2和H2O2 |
| D、H2O和SO2 |
考点:共价键的形成及共价键的主要类型
专题:化学键与晶体结构
分析:根据晶体的类型和所含化学键的类型分析,离子化合物含有离子键,可能含有共价键,共价化合物只含共价键,双原子分子或多原子分子含有共价键.
解答:
解:A.CO中C原子和O原子之间只存在共价键,MgCl2中镁离子和氯离子之间只存在离子键,两种晶体分别为分子晶体和离子晶体,故A错误;
B.NH4F存在离子键和共价键,属于离子晶体;NaF中只存在离子键,为离子晶体,故B错误;
C.Na2O2存在离子键和共价键,属于离子晶体,H2O2只存在共价键,为分子晶体,故C错误;
D.H2O中O原子和H原子之间只存在共价键,SO2中O原子和S原子之间只存在共价键,H2O和SO2的构成微粒是分子,所以都是分子晶体,故D正确;
故选D.
B.NH4F存在离子键和共价键,属于离子晶体;NaF中只存在离子键,为离子晶体,故B错误;
C.Na2O2存在离子键和共价键,属于离子晶体,H2O2只存在共价键,为分子晶体,故C错误;
D.H2O中O原子和H原子之间只存在共价键,SO2中O原子和S原子之间只存在共价键,H2O和SO2的构成微粒是分子,所以都是分子晶体,故D正确;
故选D.
点评:本题考查了化学键和晶体类型的判断,根据晶体中存在的化学键及晶体的构成微粒确定晶体类型,根据微粒之间的作用力判断化学键,题目难度不大.

练习册系列答案
相关题目
下列关于晶体与非晶体的说法不正确的是( )
| A、区别晶体与非晶体最可靠的科学方法是对固体进行x-射线衍射实验 |
| B、非晶体中粒子的排列无序,所以非晶体具有各向异性 |
| C、晶体有自范性 |
| D、非晶体无固定熔点 |
铆在铜板上的铁铆钉(如图所示),处于酸性不强的水膜中.下列有关说法正确的是( )
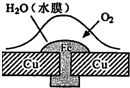

| A、铁铆钉在此环境下不易被腐蚀 |
| B、原电池反应的化学方程式:2Fe+O2+2H2O═2Fe(OH)2 |
| C、与铁接触的水膜发生反应:O2+4Fe-+2H2O═4OH- |
| D、如果在酸雨环境中,将发生:Cu-2e-═Cu2+ |
对于反应3Fe(s)+4H2O(g)?Fe3O4(s)+4H2(g)的平衡常数,下列说法正确的是( )
A、K=
| ||
B、K=
| ||
| C、增大c(H2O)或减小c(H2),会使该反应平衡常数减小 | ||
| D、改变反应的温度,平衡常数不一定变化 |
在C(s)+CO2(g)═2CO(g)的反应中,现采取下列措施:①缩小容器体积;②增加碳的量;③通入CO2;④恒容下充入N2; ⑤恒压下充入N2,能够使反应速率增大的措施是( )
| A、①④ | B、②③⑤ |
| C、①③ | D、①②④ |
下列说法中正确的是(NA表示阿伏加德罗常数的值)( )
| A、在常温常压下,11.2L N2含有的分子数为0.5NA |
| B、在常温常压下,1mol H2含有的原子数为2NA |
| C、71g Cl2的体积约为22.4L |
| D、在同温同压下,相同体积的任何气体单质所含的原子数相同 |
下列对酒精灯的使用方法的叙述错误的是( )
| A、加入酒精不超过容积的2/3 |
| B、可以用嘴吹灭火焰 |
| C、不用时须盖上灯帽 |
| D、禁止向燃着的酒精灯里添加酒精 |
下列推断正确的是( )
| A、Na2O和Na2O2组成元素相同,与CO2反应产物也相同 |
| B、SO2和CO2都是酸性氧化物,都能与NaOH溶液反应 |
| C、NO和NO2的密度均比空气大,都可用向上排空气法收集 |
| D、C3H8和CH3CH2OH相对分子质量相近,分子间作用力相近,二者沸点也相近 |
若在加入铝粉能放出H2的溶液中,分别加入下列各组离子,可能大量共存的是( )
| A、NH4+ NO3- CO32- Na+ |
| B、Na+ Ba2+ Mg2+ HCO3- |
| C、Cu2+ Fe3+ K+ Cl- |
| D、NO3- K+ AlO2- H+ |