题目内容
下列推断正确的是( )
| A、Na2O和Na2O2组成元素相同,与CO2反应产物也相同 |
| B、SO2和CO2都是酸性氧化物,都能与NaOH溶液反应 |
| C、NO和NO2的密度均比空气大,都可用向上排空气法收集 |
| D、C3H8和CH3CH2OH相对分子质量相近,分子间作用力相近,二者沸点也相近 |
考点:钠的重要化合物,氮的氧化物的性质及其对环境的影响,二氧化硫的化学性质
专题:元素及其化合物
分析:A.Na2O与CO2反应产物是碳酸钠;Na2O2与CO2反应产物为碳酸钠和氧气;
B.能够与碱反应只生成盐和水的氧化物属于酸性氧化物;
C.NO与空气密度相差不大,不能用排气法收集;
D.CH3CH2OH中存在氢键,氢键的存在物质的沸点显著升高.
B.能够与碱反应只生成盐和水的氧化物属于酸性氧化物;
C.NO与空气密度相差不大,不能用排气法收集;
D.CH3CH2OH中存在氢键,氢键的存在物质的沸点显著升高.
解答:
解:A.Na2O和Na2O2组成元素相同,与CO2反应产物不同,故A错误;
B.SO2和CO2都能够与NaOH溶液反应,且都只生成盐和水,故B正确;
C.NO与空气密度相差不大,不能用排气法收集,故C错误;
D.C3H8和CH3CH2OH相对分子质量相近,分子间作用力相近,但是因为乙醇中存在氢键,所以其沸点高于C3H8,故D错误;
故选:B.
B.SO2和CO2都能够与NaOH溶液反应,且都只生成盐和水,故B正确;
C.NO与空气密度相差不大,不能用排气法收集,故C错误;
D.C3H8和CH3CH2OH相对分子质量相近,分子间作用力相近,但是因为乙醇中存在氢键,所以其沸点高于C3H8,故D错误;
故选:B.
点评:本题考查了物质的性质,明确物质的性质、酸性氧化物的概念,氢键对物质性质的影响是解题关键,注意氢键只影响物质的物理性质.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列离子方程式正确的是( )
| A、稀硫酸滴在银片上:Ag+2H+=Ag++H2↑ |
| B、硫酸镁溶液与氢氧化钡溶液反应:Ba2++SO42-=BaSO4↓ |
| C、硝酸银溶液与盐酸反应:Ag++Cl-=AgCl↓ |
| D、澄清石灰水与碳酸钠溶液反应:Ca(OH)2+CO32-=CaCO3↓+H2O |
下列各组物质中,化学键的类型(离子键、共价键)相同的是( )
| A、CO和MgCl2 |
| B、NH4F和NaF |
| C、Na2O2和H2O2 |
| D、H2O和SO2 |
下列金属的冶炼适宜用热还原法冶炼的是( )
| A、钠 | B、铝 | C、汞 | D、铁 |
下列关于平衡常数K的说法中,正确的是( )
| A、从平衡常数K的大小能推断一个反应进行的程度 |
| B、改变反应物浓度或生成物浓度都会改变平衡常数K |
| C、平衡常数K与温度、反应浓度、压强有关 |
| D、在任何条件下,化学平衡常数是一个恒定值 |
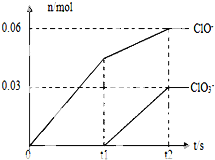 将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO3-两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示.下列说法正确的是( )
将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO3-两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示.下列说法正确的是( )| A、苛性钾溶液中KOH的物质的量是0.09mol |
| B、ClO3-的生成是由于氯气的量的多少引起的 |
| C、在酸性条件下,ClO-和ClO3-可生成Cl2 |
| D、反应中转移电子的物质的量是0.21mol |
水的电离过程为H2O?H++OH-,下列叙述正确的是( )
| A、升高温度,促进水的电离,c(H+)增大,PH增大 |
| B、加入NaOH,抑制水的电离,c(H+)和c(OH-)都减小 |
| C、加入NH4Cl,促进水的电离,溶液呈碱性 |
| D、Kw只与温度有关 |
下列方程式书写正确的是( )
| A、向小苏打溶液中加入NaAlO2:AlO2-+HCO3-+H2O=Al(OH)3↓+CO32- |
| B、碳酸氢钠溶液跟过量的饱和石灰水反应:2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O |
| C、NaHSO4溶液中滴入少量Ba(OH)2:H++SO42-+Ba2++OH-=BaSO4↓+H2O |
| D、200mL2mol/LFeBr2溶液中通入11.2L标况下的Cl2:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl-? |