题目内容
6.向50mLNa2SO4和Na2CO3的混合溶液中加入过量的BaCl2溶液,得到14.51g白色沉淀,向白色沉淀中加入过量的稀HNO3,充分反应后,沉淀减少到4.66g,并有气体产生.(1)原混合溶液中Na2SO4的物质的量浓度是多少?
(2)产生的气体在标准状况下的体积是多少?
(3)原溶液中Na+物质的量浓度是多少?
分析 向50mL Na2SO4和Na2CO3的混合溶液中加入过量的BaCl2溶液,得到14.51g白色沉淀,得到的白色沉淀是BaCO3、BaSO4,向白色沉淀中加入过量的稀HNO3,充分反应后,沉淀减少到4.66g,剩余的沉淀是BaSO4,碳酸钡溶解,n(BaSO4)=$\frac{4.66g}{233g/mol}$=0.02mol,n(BaCO3)=$\frac{14.51g-4.66g}{197g/mol}$=0.05mol,
(1)根据S原子守恒得n(Na2SO4)=n(BaSO4)=0.02mol,则c(Na2SO4)=$\frac{n}{V}$;
(2)根据C原子守恒得n(CO2)=n(BaCO3)=0.05mol,根据V=nVm;
(3)根据Na原子守恒得n(Na+)=2n( Na2SO4)+2n(Na2CO3),c(Na+)=$\frac{n}{V}$.
解答 解:向50mL Na2SO4和Na2CO3的混合溶液中加入过量的BaCl2溶液,得到14.51g白色沉淀,得到的白色沉淀是BaCO3、BaSO4,向白色沉淀中加入过量的稀HNO3,充分反应后,沉淀减少到4.66g,剩余的沉淀是BaSO4,碳酸钡溶解,n(BaSO4)=$\frac{4.66g}{233g/mol}$=0.02mol,n(BaCO3)=$\frac{14.51g-4.66g}{197g/mol}$=0.05mol,
(1)根据S原子守恒得n(Na2SO4)=n(BaSO4)=0.02mol,则c(Na2SO4)=$\frac{n}{V}$=$\frac{0.02mol}{0.05L}$=0.4mol/L,
答:硫酸钠的物质的量浓度是0.4mol/L;
(2)根据C原子守恒得n(CO2)=n(BaCO3)=0.05mol,根据V=nVm=0.05mol×22.4L/mol=1.12L,
答:生成二氧化碳体积为1.12L;
(3)根据Na原子守恒得n(Na+)=2n( Na2SO4)+2n(Na2CO3)=2×0.02mol+2×0.05mol=0.14mol,c(Na+)=$\frac{n}{V}$=$\frac{0.14mol}{0.05L}$=2.8mol/L,
答:钠离子浓度是2.8mol/L.
点评 本题考查混合物的计算,为高频考点,侧重考查学生分析计算能力,明确各个物理量之间的关系是解本题关键,注意原子守恒的灵活运用,熟练掌握物质的量有关公式,题目难度不大.

| A. | Fe3+、NO3-、SO42-、Na+ | B. | Ca2+、H+、Cl-、HCO3- | ||
| C. | NH4+、Al3+、NO3-、OH- | D. | Ba2+、ClO-、SO42-、SCN- |
| A. | 7.5% | B. | 大于7.5%. | C. | 小于7.5% | D. | 无法确定 |
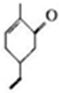 .下列有关M的说法正确的是( )
.下列有关M的说法正确的是( )| A. | 可以发生氧化反应 | B. | 分子式C9H10O | ||
| C. | 分子中所有原子都处子同一平面上 | D. | 不能使溴的四氯化碳溶液褪色 |
(1)已知石墨的标准燃烧热为y kJ•mol-1,1.2g石墨在1.68L(标准状况)氧气中燃烧,至反应物耗尽,放出x kJ热量,则石墨与氧气反应生成CO的热化学方程式为C(s)+$\frac{1}{2}$O2(g)=CO(g)△H=-(20x-y)kJ•mol-1.
(2)二氧化碳合成甲醇是碳减排的新方向,将CO2转化为甲醇的热化学方程式为:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H
①该反应的平衡常数表达式为K=$\frac{C(CH{\;}_{3}OH)C(H{\;}_{2}O)}{C(CO{\;}_{2})C{\;}^{3}(H{\;}_{2})}$.
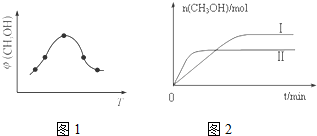
②取五份等体积CO2和H2的混合气体(物质的量之比均为1:3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数φ(CH3OH)与反应温度T的关系曲线如图1所示,则上述CO2转化为甲醇反应的△H<(填“>”“<”或“=”)0.
③在两种不同温度下发生反应,测得CH3OH的物质的量随时间变化如图2所示,曲线I、Ⅱ对应的平衡常数大小关系为KⅠ>KⅡ(填“>”“<”或“=”).
④一定温度下,在容积相同且固定的两个密闭容器中,按如下方式投入反应物,一段时间后达到平衡.
| 容 器 | 甲 | 乙 |
| 反应物投入量 | 1molCO2 3molH2 | a molCO2、b molH2、c molCH3OH(g)、c molH2O(g) (a、b、c均不等于0) |
| A. | 6.02×1023 | B. | 6.02×1022 | C. | 6.02×1021 | D. | 6.02×1020 |
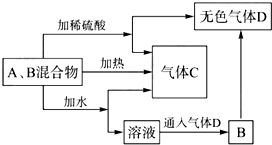 有A、B两种常见化合物,其焰色反应均呈黄色,C是一种单质气体,相互转化关系如图所示(其他物质均已略去).回答下列问题:
有A、B两种常见化合物,其焰色反应均呈黄色,C是一种单质气体,相互转化关系如图所示(其他物质均已略去).回答下列问题: