题目内容
氨气是工农业生产不可或缺的化工原料.
(1)工业上合成氨选择500℃左右高温而非常温进行的主要目的是 ;
(2)氨用于工业制硝酸的主反应为:
4NH3(g)+5O2(g)?4NO(g)+6H2O(g),△H=mkJ/mol(m<0)
在容积固定的VL恒温密闭容器中充入反应物发生上述反应,容器内部分物质的物质的量浓度如表:
①下列能说明该反应已经达到平衡状态的是
A.容器中气体平均摩尔质量不变 B.c (O2)不变
C.v(O2)=1.25v(NH3) D.体系气体无颜色变化
E.体系压强不变
②反应在第2min时,容器中压强与反应前之比为19:18,则a= mol/L在0~2min时,容器内放出能量为 kJ;
③反应在第4min时改变了条件,改变的条件最可能是 ;此时v(正) (填“增大”、“减小”或“不变”);
④若在容积固定的绝热密闭容器中发生上述反应,其余条件不变,在0~2min时其平均速率与原来相比 (填“增大”、“减小”或“不变”,下同),平衡时的转化率与原来相比 .
(1)工业上合成氨选择500℃左右高温而非常温进行的主要目的是
(2)氨用于工业制硝酸的主反应为:
4NH3(g)+5O2(g)?4NO(g)+6H2O(g),△H=mkJ/mol(m<0)
在容积固定的VL恒温密闭容器中充入反应物发生上述反应,容器内部分物质的物质的量浓度如表:
| 时间/浓度 | c(NH3)(mol/L) | c(O2)(mol/L) | c(NO)(mol/L) |
| 起始 | 0.800 | 1.000 | 0.000 |
| 第2min | a | b | c |
| 第4min | 0.400 | 0.500 | |
| 第6 min | 0.700 | 0.625 | 0.120 |
A.容器中气体平均摩尔质量不变 B.c (O2)不变
C.v(O2)=1.25v(NH3) D.体系气体无颜色变化
E.体系压强不变
②反应在第2min时,容器中压强与反应前之比为19:18,则a=
③反应在第4min时改变了条件,改变的条件最可能是
④若在容积固定的绝热密闭容器中发生上述反应,其余条件不变,在0~2min时其平均速率与原来相比
分析:(1)根据温度、压强、催化剂对可逆反应4NH3(g)+5O2(g)?4NO(g)+6H2O(g)的影响进行分析;
(2)①根据达到平衡状态,一定满足正逆反应速率相等,各组分的浓度、百分含量不再变化进行判断;
②设在第2min时转化了xmol氨气,压强之比等于气体物质的量之比,根据反应在第2min时,容器中压强与反应前之比为19:18计算出a;根据消耗4mol氨气放出-mkJ热量计算出该反应放出的热量;
③根据表中数据反应物浓度都增大判断平衡移动分析及改变的条件;根据平衡移动分析判断正反应速率变化;
④根据该反应为放热反应,反应过程中温度升高,此条件下比原平衡温度高进行分析反应速率变化及转化率变化.
(2)①根据达到平衡状态,一定满足正逆反应速率相等,各组分的浓度、百分含量不再变化进行判断;
②设在第2min时转化了xmol氨气,压强之比等于气体物质的量之比,根据反应在第2min时,容器中压强与反应前之比为19:18计算出a;根据消耗4mol氨气放出-mkJ热量计算出该反应放出的热量;
③根据表中数据反应物浓度都增大判断平衡移动分析及改变的条件;根据平衡移动分析判断正反应速率变化;
④根据该反应为放热反应,反应过程中温度升高,此条件下比原平衡温度高进行分析反应速率变化及转化率变化.
解答:解:(1)4NH3(g)+5O2(g)?4NO(g)+6H2O(g),该反应是气体体积减小、放热的可逆反应,要使平衡向正反应方向移动,应降低温度、增大压强,但温度过低反应速率过小,不利于工业生成效益;温度越高,反应速率越大,所以应适当升高温度,使反应速率增大;使用催化剂也能增大反应速率,但在500℃左右时催化剂的活性最大,所以选择采用500℃左右的温度进行,
故答案为:在此温度下催化剂的活性最大;
(2)①A.该反应是体积减小的反应,气体的总物质的量在达到平衡状态之前是变量,气体的质量不变,若容器中气体平均摩尔质量不变,说明正逆反应速率相等,达到了平衡状态,故A正确;
B.c (O2)不变,说明正逆反应速率相等,达到了平衡状态,故B正确;
C.v(O2)=1.25v(NH3),没有告诉是正逆反应速率,无法判断是否达到平衡状态,故C错误;
D.该反应过程中混合气体始终为无色,无法根据颜色变化判断平衡状态,故D错误;
E.该反应是体积缩小的反应,反应过程中气体的物质的量逐渐减小,压强逐渐减小,若体系压强不变,说明正逆反应速率相等,达到了平衡状态,故E正确;
故选ABE;
②设第2min消耗了xmol氨气,根据反应方程式4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△c
4 5 4 6 1
x
x
反应后混合气体的浓度为:(0.800+1.000+0.25x)mol/L,根据气体物质的量之比等于压强之比可知,
=
,
解得:x=0.400,则a=0.800-0.400=0.400;反应消耗氨气的物质的量为:0.400mol/L×V=0.4Vmol,放出的热量为:-m×
=0.1mVkJ,
故答案为:0.4;-0.1Vm;
③由表中数据可知,反应物浓度增大,说明平衡向着逆向移动,该反应为放热反应,所以应该是降低了温度;平衡向着逆向移动,正逆反应速率都会减小,
硅答案为:降低温度;减小;
④由于该反应为放热反应,若在容积固定的绝热密闭容器中发生上述反应,其余条件不变,反应过程中反应体系的温度高于原反应,所以正逆反应速率都增大;由于温度升高,平衡向着逆向移动,所以反应物的转化率会减小,
故答案为:增大;减小.
故答案为:在此温度下催化剂的活性最大;
(2)①A.该反应是体积减小的反应,气体的总物质的量在达到平衡状态之前是变量,气体的质量不变,若容器中气体平均摩尔质量不变,说明正逆反应速率相等,达到了平衡状态,故A正确;
B.c (O2)不变,说明正逆反应速率相等,达到了平衡状态,故B正确;
C.v(O2)=1.25v(NH3),没有告诉是正逆反应速率,无法判断是否达到平衡状态,故C错误;
D.该反应过程中混合气体始终为无色,无法根据颜色变化判断平衡状态,故D错误;
E.该反应是体积缩小的反应,反应过程中气体的物质的量逐渐减小,压强逐渐减小,若体系压强不变,说明正逆反应速率相等,达到了平衡状态,故E正确;
故选ABE;
②设第2min消耗了xmol氨气,根据反应方程式4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△c
4 5 4 6 1
x
| 1 |
| 4 |
反应后混合气体的浓度为:(0.800+1.000+0.25x)mol/L,根据气体物质的量之比等于压强之比可知,
| (0.800+1.000+0.25x)mol/L |
| (0.800+1.000)mol/L |
| 19 |
| 18 |
解得:x=0.400,则a=0.800-0.400=0.400;反应消耗氨气的物质的量为:0.400mol/L×V=0.4Vmol,放出的热量为:-m×
| 0.4Vmol |
| 4mol |
故答案为:0.4;-0.1Vm;
③由表中数据可知,反应物浓度增大,说明平衡向着逆向移动,该反应为放热反应,所以应该是降低了温度;平衡向着逆向移动,正逆反应速率都会减小,
硅答案为:降低温度;减小;
④由于该反应为放热反应,若在容积固定的绝热密闭容器中发生上述反应,其余条件不变,反应过程中反应体系的温度高于原反应,所以正逆反应速率都增大;由于温度升高,平衡向着逆向移动,所以反应物的转化率会减小,
故答案为:增大;减小.
点评:本题考查了化学平衡状态的判断、化学平衡的影响因素、化学平衡的计算等知识,题目难度中等,注意掌握判断化学平衡状态的方法、明确影响化学平衡的因素.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
氨气在工农业生产中有重要的用途.某化学小组试图制备纯净氨气并验证其某些性质.
(1)下列是所给的部分仪器:
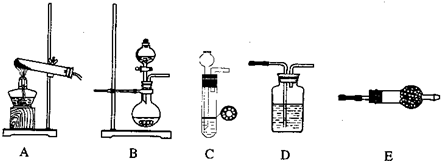
所给的药品有:a.氯化铵溶液b.碱石灰c.浓氨水d.浓硫酸e.氯化钙
根据以上所给仪器和药品,选用合理编号,完成下表.
(2)如图装置中的实验现象是 ,硬质玻璃管中发生反应的化学方程式为 .
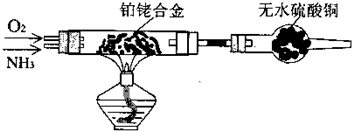
(3)如将氨气不断通入滴有酚酞的AgNO3溶液中,现象为 ,反应结束所得溶液中的离子主要有(写离子符号) .
(1)下列是所给的部分仪器:

所给的药品有:a.氯化铵溶液b.碱石灰c.浓氨水d.浓硫酸e.氯化钙
根据以上所给仪器和药品,选用合理编号,完成下表.
| 制备NH3 | 干燥 | 化学方程式 | ||
| 仪器 | 药品 | 仪器 | 药品 | |

(3)如将氨气不断通入滴有酚酞的AgNO3溶液中,现象为
氨气在工农业生产中有重要的用途.某校甲、乙两个化学小组分别对氨的相关实验进行了研究.
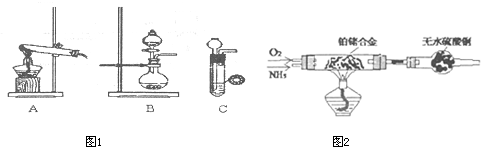
(1)甲、乙两小组选择了不同方法制(图1)取氨气,请将实验装置的字母编号和制备原理填写在下表空
格中.
(2)甲组通过图2装置(尾气处理装置已略去)验证了氨有还原性,装置中的实验现象是 ,硬质玻璃管中氨发生催化氧化反应的化学方程式为 .
(3)甲组将足量氨气不断通入滴有酚酞的AgNO3溶液中,现象为 ,反应结束所得溶液中除了H+、OH-、NH4+外还主要含有的离子有 .
(4)乙组欲制备氮化镁,查阅资料发现氨跟氧化铜反应可以制备氮气(2NH3+3CuO
3Cu+N2+3H2O),而氮气跟镁在高温下反应可得到氮化镁,但氮化镁遇水立即反应生成Mg(OH)2和NH3.乙组提出了如下制备氮化镁的实验方案示意框图(实验前系统内空气已排除;图中箭头表示气体的流向).你认为此方案是否正确,并说明理由 .
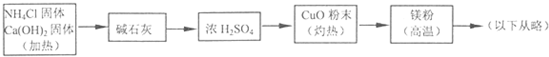

(1)甲、乙两小组选择了不同方法制(图1)取氨气,请将实验装置的字母编号和制备原理填写在下表空
格中.
| 实验装置 | 实验药品 | 制备原理 | |
| 甲小组 | A | 氢氧化钙、氯化铵 | 反应的化学方程式为 ① |
| 乙小组 | ② |
浓氨水、氢氧化钠 | 用化学平衡原理分析氢氧化钠的作用: ③ |
(3)甲组将足量氨气不断通入滴有酚酞的AgNO3溶液中,现象为
(4)乙组欲制备氮化镁,查阅资料发现氨跟氧化铜反应可以制备氮气(2NH3+3CuO
| ||