题目内容
氨气在工农业生产中有重要应用.(1)①氮气用于工业合成氨,写出氮气的电子式
(2)如图所示,向NaOH固体上滴几滴浓氨水,迅速盖上盖,观察现象.

①浓盐酸液滴附近会出现白烟,发生反应的化学方程式为
②浓硫酸液滴上方没有明显现象,一段时间后浓硫酸的液滴中有白色固体,该固体可能是
③FeSO4液滴中先出现灰绿色沉淀,过一段时间后变成红褐色,发生的反应包括Fe2++2NH3?H2O═Fe(OH)2↓+2NH4+和
(3)空气吹脱法是目前消除NH3对水体污染的重要方法.在一定条件下,向水体中加入适量NaOH可使NH3的脱除率增大,用平衡移动原理解释其原因
(4)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸(HNO2),反应的化学方程式为
分析:(1)①氮气中N原子满足最外层8电子稳定结构,存在N≡N;
②非金属性越强,气态氢化物越稳定;
(2)①浓盐酸液滴附近会出现白烟,发生HCl与氨气的反应生成氯化铵;
②浓硫酸难挥发,能与氨气反应生成硫酸盐;
③FeSO4与碱反应生成白色沉淀,然后出现灰绿色沉淀,过一段时间后变成红褐色,氢氧化亚铁被氧化;
(3)结合NH3+H2O NH3?H2O
NH3?H2O NH4++OH-及平衡移动分析;
NH4++OH-及平衡移动分析;
(5)氨能够被氧气氧化生成亚硝酸(HNO2),由质量守恒定律可知还生成水;结合元素的化合价变化计算.
②非金属性越强,气态氢化物越稳定;
(2)①浓盐酸液滴附近会出现白烟,发生HCl与氨气的反应生成氯化铵;
②浓硫酸难挥发,能与氨气反应生成硫酸盐;
③FeSO4与碱反应生成白色沉淀,然后出现灰绿色沉淀,过一段时间后变成红褐色,氢氧化亚铁被氧化;
(3)结合NH3+H2O
 NH3?H2O
NH3?H2O NH4++OH-及平衡移动分析;
NH4++OH-及平衡移动分析;(5)氨能够被氧气氧化生成亚硝酸(HNO2),由质量守恒定律可知还生成水;结合元素的化合价变化计算.
解答:解:(1)①氮气中N原子满足最外层8电子稳定结构,存在N≡N,则氮气的电子式为 ,故答案为:
,故答案为: ;
;
②非金属性N>P,则NH3的稳定性比PH3强,故答案为:强;
(2)①浓盐酸液滴附近会出现白烟,发生HCl与氨气的反应生成氯化铵,该反应为NH3+HCl═NH4Cl,故答案为:NH3+HCl═NH4Cl;
②浓硫酸难挥发,能与氨气反应生成硫酸盐,则一段时间后浓硫酸的液滴中生成的白色固体为NH4HSO4或(NH4)2SO4,故答案为:NH4HSO4或(NH4)2SO4;
③FeSO4与碱反应生成白色沉淀,发生反应为Fe2++2NH3?H2O═Fe(OH)2↓+2NH4+,然后出现灰绿色沉淀,过一段时间后变成红褐色,是因氢氧化亚铁被氧化,发生反应为4Fe(OH)2+O2+2H2O═4Fe(OH)3,
故答案为:4Fe(OH)2+O2+2H2O═4Fe(OH)3;
(3)在一定条件下,向水体中加入适量NaOH可使NH3的脱除率增大,是因氨在水中存在平衡为NH3+H2O NH3?H2O
NH3?H2O NH4++OH-,加入NaOH后OH-浓度增大平衡逆向移动,故有利于氨的脱除,
NH4++OH-,加入NaOH后OH-浓度增大平衡逆向移动,故有利于氨的脱除,
故答案为:氨在水中存在平衡为NH3+H2O NH3?H2O
NH3?H2O NH4++OH-,加入NaOH后OH-浓度增大平衡逆向移动,故有利于氨的脱除;
NH4++OH-,加入NaOH后OH-浓度增大平衡逆向移动,故有利于氨的脱除;
(4)氨能够被氧气氧化生成亚硝酸(HNO2),由质量守恒定律可知还生成水,该反应为2NH3+3O2
2HNO2+2H2O,由反应可知,生成2molHNO2时转移2mol×[3-(-3)]=12mol电子,则有0.3mol电子发生转移时,生成亚硝酸0.3mol×
=0.05mol,其质量为0.05mol×47g/mol=2.35 g,
故答案为:2NH3+3O2
2HNO2+2H2O;2.35.
 ,故答案为:
,故答案为: ;
; ②非金属性N>P,则NH3的稳定性比PH3强,故答案为:强;
(2)①浓盐酸液滴附近会出现白烟,发生HCl与氨气的反应生成氯化铵,该反应为NH3+HCl═NH4Cl,故答案为:NH3+HCl═NH4Cl;
②浓硫酸难挥发,能与氨气反应生成硫酸盐,则一段时间后浓硫酸的液滴中生成的白色固体为NH4HSO4或(NH4)2SO4,故答案为:NH4HSO4或(NH4)2SO4;
③FeSO4与碱反应生成白色沉淀,发生反应为Fe2++2NH3?H2O═Fe(OH)2↓+2NH4+,然后出现灰绿色沉淀,过一段时间后变成红褐色,是因氢氧化亚铁被氧化,发生反应为4Fe(OH)2+O2+2H2O═4Fe(OH)3,
故答案为:4Fe(OH)2+O2+2H2O═4Fe(OH)3;
(3)在一定条件下,向水体中加入适量NaOH可使NH3的脱除率增大,是因氨在水中存在平衡为NH3+H2O
 NH3?H2O
NH3?H2O NH4++OH-,加入NaOH后OH-浓度增大平衡逆向移动,故有利于氨的脱除,
NH4++OH-,加入NaOH后OH-浓度增大平衡逆向移动,故有利于氨的脱除,故答案为:氨在水中存在平衡为NH3+H2O
 NH3?H2O
NH3?H2O NH4++OH-,加入NaOH后OH-浓度增大平衡逆向移动,故有利于氨的脱除;
NH4++OH-,加入NaOH后OH-浓度增大平衡逆向移动,故有利于氨的脱除;(4)氨能够被氧气氧化生成亚硝酸(HNO2),由质量守恒定律可知还生成水,该反应为2NH3+3O2
| ||
| 2 |
| 12 |
故答案为:2NH3+3O2
| ||
点评:本题以氨气的性质考查物质之间的反应,涉及氧化还原反应、平衡移动原理、非金属性比较等,综合性较强,侧重学生分析能力和计算能力的考查,注意知识的迁移应用,题目难度中等.

练习册系列答案
相关题目


 (1)硫酸生产中,SO2催化氧化生成SO3:2SO2(g)+O2(g) 2SO3(g),混合体系中SO3的百分含量和温度的关系如下图所示(曲线上任何一点都表示平衡状态)。根据图示回答下列问题:
(1)硫酸生产中,SO2催化氧化生成SO3:2SO2(g)+O2(g) 2SO3(g),混合体系中SO3的百分含量和温度的关系如下图所示(曲线上任何一点都表示平衡状态)。根据图示回答下列问题: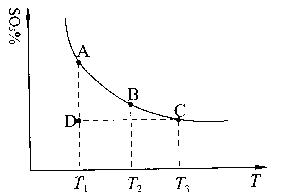

 (填“>”、“<”或“=”)
(填“>”、“<”或“=”) )
) 2SO3(g),混合体系中SO3的百分含量和温度的关系如下图所示(曲线上任何一点都表示平衡状态)。根据图示回答下列问题:
2SO3(g),混合体系中SO3的百分含量和温度的关系如下图所示(曲线上任何一点都表示平衡状态)。根据图示回答下列问题:

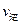 (填“>”、“<”或“=”)
(填“>”、“<”或“=”) )
) 2SO3(g),混合体系中SO3的百分含量和温度的关系如下图所示(曲线上任何一点都表示平衡状态)。根据图示回答下列问题:
2SO3(g),混合体系中SO3的百分含量和温度的关系如下图所示(曲线上任何一点都表示平衡状态)。根据图示回答下列问题:
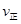
 (填“>”、“<”或“=”)(2)氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。
(填“>”、“<”或“=”)(2)氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。
 )
)