题目内容
25℃时,pH=a的NaOH溶液中,溶液的C(OH-)= mol/L.
考点:pH的简单计算
专题:电离平衡与溶液的pH专题
分析:根据H2O?H++OH-知,NaOH溶液中,氢离子浓度仅由水电离产生,根据pH=-lgc(H+),结合Kw=c(H+)×c(OH-),求解溶液的C(OH-).
解答:
解:pH=-lgc(H+),pH=a的NaOH溶液中,c(H+)=1×10-amol/L,Kw=c(H+)×c(OH-),溶液的C(OH-)=
mol/L=10a-14mol/L,
故答案为:10a-14.
| 10-14 |
| 10-a |
故答案为:10a-14.
点评:本题考查了pH的简单计算,明确氢离子与氢氧根离子浓度的关系是解本题的关键,题目难度不大.

练习册系列答案
相关题目
下列装置能达到实验目的是( )
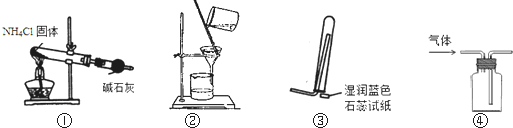

| A、用①装置制取干燥的氨气 |
| B、用②装置除去淀粉溶液中的NaCl |
| C、③装置可用于氨气的收集、检验 |
| D、④装置可用排空气法收集氢气 |

 在容积相同的不同密闭容器内,分别充入同量的N2和H2,在不同温度,任其发生反应N2+3H2?2NH3,在第7秒时分别测定其中NH3的体积分数φ(NH3),并绘成如图曲线.
在容积相同的不同密闭容器内,分别充入同量的N2和H2,在不同温度,任其发生反应N2+3H2?2NH3,在第7秒时分别测定其中NH3的体积分数φ(NH3),并绘成如图曲线.
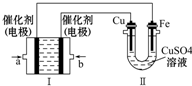 甲烷作为一种新能源在化学领域应用广泛,请回答下列问题:
甲烷作为一种新能源在化学领域应用广泛,请回答下列问题: