题目内容
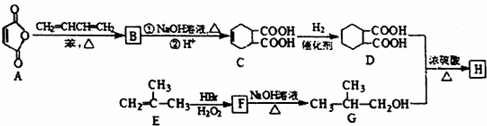
如图1所示是某些物质的转化关系图(个别小分子产物可能没有标出).

已知:
Ⅰ.A、B、C是三种常见的气态含碳化合物,A、B的相对分子质量均为28,C的相对分子质量略小于A.
Ⅱ.化合物D的比例模型如图2所示;D完全燃烧时,消耗的氧气与生成的CO2的体积比为1:1.
Ⅲ.硫酸氢乙酯水解得E与硫酸,从A经硫酸氢乙酯至E的反应中,硫酸实际起到了催化剂的作用.
Ⅳ.E与F反应,得一种有浓郁香味的油状液体G,E与D反应得无色液体H,在反应②、③中,参与反应的官能团完全相同.
请按要求回答下列问题:
(1)化合物D所含官能团的名称是 ,化合物C的结构简式为 .
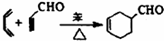
(2)反应①的反应类型是 ,化合物A与F在一定条件下也可发生类似①的反应,其化学方程式为 .
(3)化合物H可进一步聚合成某种柔软且透明的高分子化合物,写出其化学反应方程式 .

已知:
Ⅰ.A、B、C是三种常见的气态含碳化合物,A、B的相对分子质量均为28,C的相对分子质量略小于A.
Ⅱ.化合物D的比例模型如图2所示;D完全燃烧时,消耗的氧气与生成的CO2的体积比为1:1.
Ⅲ.硫酸氢乙酯水解得E与硫酸,从A经硫酸氢乙酯至E的反应中,硫酸实际起到了催化剂的作用.
Ⅳ.E与F反应,得一种有浓郁香味的油状液体G,E与D反应得无色液体H,在反应②、③中,参与反应的官能团完全相同.
请按要求回答下列问题:
(1)化合物D所含官能团的名称是
(2)反应①的反应类型是
(3)化合物H可进一步聚合成某种柔软且透明的高分子化合物,写出其化学反应方程式
考点:有机物的推断
专题:
分析:化合物D的比例模型如图2所示,D完全燃烧时,消耗的氧气与生成的CO2的体积比为1:1,则D为CH2=CHCOOH,硫酸氢乙酯水解得E与硫酸,则E为CH3CH2OH,从A经硫酸氢乙酯至E的反应中,硫酸实际起到了催化剂的作用,A的相对分子质量为28,可推知A为CH2=CH2,E与F反应,得一种有浓郁香味的油状液体G,则F为CH3COOH,G为CH3COOCH2CH3,E与D反应得无色液体H,则H为CH2=CHCOOCH2CH3,在反应②、③中,参与反应的官能团完全相同,都是羟基和羧基发生酯化反应,A、B、C是三种常见的气态含碳化合物,A、B的相对分子质量均为28,C的相对分子质量略小于A,且B和C反应生成D,则B为CO,C为CH≡CH,据此答题.
解答:
解:化合物D的比例模型如图2所示,D完全燃烧时,消耗的氧气与生成的CO2的体积比为1:1,则D为CH2=CHCOOH,硫酸氢乙酯水解得E与硫酸,则E为CH3CH2OH,从A经硫酸氢乙酯至E的反应中,硫酸实际起到了催化剂的作用,A的相对分子质量为28,可推知A为CH2=CH2,E与F反应,得一种有浓郁香味的油状液体G,则F为CH3COOH,G为CH3COOCH2CH3,E与D反应得无色液体H,则H为CH2=CHCOOCH2CH3,在反应②、③中,参与反应的官能团完全相同,都是羟基和羧基发生酯化反应,A、B、C是三种常见的气态含碳化合物,A、B的相对分子质量均为28,C的相对分子质量略小于A,且B和C反应生成D,则B为CO,C为CH≡CH,
(1)根据上面的分析可知,D为CH2=CHCOOH,D所含官能团的名称是碳碳双键和羧基,C为CH≡CH,
故答案为:碳碳双键和羧基;CH≡CH;
(2)反应①的反应类型是硫酸与乙烯的加成反应,A为CH2=CH2,F为CH3COOH,A与F在一定条件下也可发生类似①的反应,其化学方程式为CH3COOH+CH2=CH2→CH3COOCH2CH3,
故答案为:加成;CH3COOH+CH2=CH2→CH3COOCH2CH3;
(3)H为CH2=CHCOOCH2CH3,H可进一步聚合成某种柔软且透明的高分子化合物,其化学反应方程式为 ,
,
故答案为: .
.
(1)根据上面的分析可知,D为CH2=CHCOOH,D所含官能团的名称是碳碳双键和羧基,C为CH≡CH,
故答案为:碳碳双键和羧基;CH≡CH;
(2)反应①的反应类型是硫酸与乙烯的加成反应,A为CH2=CH2,F为CH3COOH,A与F在一定条件下也可发生类似①的反应,其化学方程式为CH3COOH+CH2=CH2→CH3COOCH2CH3,
故答案为:加成;CH3COOH+CH2=CH2→CH3COOCH2CH3;
(3)H为CH2=CHCOOCH2CH3,H可进一步聚合成某种柔软且透明的高分子化合物,其化学反应方程式为
 ,
,故答案为:
 .
.
点评:本题考查有机物推断,根据题中信息结合有机物结构及相互转化关系进行推断,从而得出各有机化合物的结构,是对有机化学基础知识的综合考查,需要学生熟练掌握分子结构中的官能团,抓官能团性质进行解答,难度中等.

练习册系列答案
 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目
已知X、Y、Z、W为短周期主族元素,在周期表中的相对位置如图所示,下列说法正确的是( )
| X | Y |
| Z | W |
| A、若HmXOn为强酸,则X的氢化物溶于水一定显酸性(m、n为正整数) |
| B、若四种元素均为金属,则Z的最高价氧化物对应的水化物一定为强碱 |
| C、若四种元素均为非金属,则W的最高价氧化物对应的水化物一定是强酸 |
| D、若四种元素只有一种为金厲,则Z、Y 二者的最高价氧化物对应的水化物一定能发生反应 |
 如图是实验室制取气体的装置,其中发生装置相同,干燥和集气装置有两套,分别用图1和图2表示.下列选项中正确的是( )
如图是实验室制取气体的装置,其中发生装置相同,干燥和集气装置有两套,分别用图1和图2表示.下列选项中正确的是( )| 选项 | 发生装置中的药品 | 干燥和集气装置 |
| A | 亚硫酸钠和稀盐酸 | 图2 |
| B | 大理石和稀盐酸 | 图1 |
| C | 铜和稀硝酸 | 图2 |
| D | 氧化钙和浓氨水 | 图1 |
| A、A | B、B | C、C | D、D |
下列化学用语表示正确的是( )
A、S2-的离子结构示意图: |
| B、次氯酸的结构式:H-O-Cl |
C、水分子的比例模型: |
D、NCl3的电子式: |
某溶液中可能含有K+、NH4+、Ba2+、SO42-、I-、Cl-、NO3-中的几种,将此溶液分成两等份,进行如下实验:
①在一份溶液中加入足量NaOH,加热,可收集到标准状态下的气体1.12L;
②在另一份溶液中加入足量Ba(NO3)2溶液,有白色沉淀产生,过滤得到沉淀2.33g;
③在②的滤液中加入足量AgNO3溶液,又有4.7g沉淀产生.
有关该溶液中离子种类(不考虑H+和OH-)的判断正确的是( )
①在一份溶液中加入足量NaOH,加热,可收集到标准状态下的气体1.12L;
②在另一份溶液中加入足量Ba(NO3)2溶液,有白色沉淀产生,过滤得到沉淀2.33g;
③在②的滤液中加入足量AgNO3溶液,又有4.7g沉淀产生.
有关该溶液中离子种类(不考虑H+和OH-)的判断正确的是( )
| A、溶液中至少有2种阳离子 |
| B、只能确定溶液中NH4+、SO42-是否存在 |
| C、溶液中最多有4种阴离子 |
| D、溶液中不可能同时存在K+和NO3- |
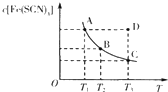 已知:FeCl3(aq)+3KSCN(aq)?3KCl(aq)+Fe(SCN)3(aq),平衡时Fe(SCN)3的物质的量浓度与温度T的关系如图所示,则下列说法正确的是( )
已知:FeCl3(aq)+3KSCN(aq)?3KCl(aq)+Fe(SCN)3(aq),平衡时Fe(SCN)3的物质的量浓度与温度T的关系如图所示,则下列说法正确的是( )| A、A点与B点相比,A点的c( Fe3+)大 |
| B、加入KCl固体可以使溶液由D点变到C点 |
| C、反应处于D点时,一定有υ(正)<υ(逆) |
| D、若T1、T2温度下的平衡常数分别为K1、K2,则K1<K2 |
 2NH3(g) ΔH=-92.4 kJ·mol-1,在反应过程中,正反应速率的变化如图
2NH3(g) ΔH=-92.4 kJ·mol-1,在反应过程中,正反应速率的变化如图


 (-R1、-R2-表示氢原子或烃基)
(-R1、-R2-表示氢原子或烃基)