题目内容
化学用语是化学学科的特色语言,化学用语可以准确表述化学现象、变化以及本质.完成下列有关方程式.
(1)Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO42-,常用作脱氯剂,该反应的离子方程式为 ;
(2)酸性高锰酸钾溶液与过氧化氢溶液反应的离子方程式: .
(3)化学反应多姿多彩,把SO2通入硝酸铁溶液中,溶液由棕黄色变为浅绿色,但立即又变为棕黄色,此时向溶液中滴加氯化钡溶液,有白色沉淀产生.请写出上述变化中溶液由棕黄色变为浅绿色,但立即又变为棕黄色所涉及的两个离子方程式: 、 .
(4)向含有n mol 溴化亚铁的溶液中通入等物质的量的氯气,请写出离子方程式: .
(1)Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO42-,常用作脱氯剂,该反应的离子方程式为
(2)酸性高锰酸钾溶液与过氧化氢溶液反应的离子方程式:
(3)化学反应多姿多彩,把SO2通入硝酸铁溶液中,溶液由棕黄色变为浅绿色,但立即又变为棕黄色,此时向溶液中滴加氯化钡溶液,有白色沉淀产生.请写出上述变化中溶液由棕黄色变为浅绿色,但立即又变为棕黄色所涉及的两个离子方程式:
(4)向含有n mol 溴化亚铁的溶液中通入等物质的量的氯气,请写出离子方程式:
考点:离子方程式的书写
专题:
分析:(1)Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO42-,则氯气被还原为氯离子;
(2)发生氧化还原反应,生成锰离子、氧气、水;
(3)SO2通入硝酸铁溶液中,溶液由棕黄色变为浅绿色,铁离子与二氧化硫发生氧化还原反应生成硫酸根离子、亚铁离子;立即又变为棕黄色,是因亚铁离子与硝酸根离子、氢离子发生氧化还原反应生成铁离子;
(4)亚铁离子、溴离子均具有还原性,但亚铁离子还原性强,与等物质的量的氯气反应,亚铁离子全部被氧化,而溴离子一半被氧化.
(2)发生氧化还原反应,生成锰离子、氧气、水;
(3)SO2通入硝酸铁溶液中,溶液由棕黄色变为浅绿色,铁离子与二氧化硫发生氧化还原反应生成硫酸根离子、亚铁离子;立即又变为棕黄色,是因亚铁离子与硝酸根离子、氢离子发生氧化还原反应生成铁离子;
(4)亚铁离子、溴离子均具有还原性,但亚铁离子还原性强,与等物质的量的氯气反应,亚铁离子全部被氧化,而溴离子一半被氧化.
解答:
解:(1)Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO42-,则氯气被还原为氯离子,离子反应为S2O32-+4Cl2+5H2O═2SO42-+8Cl-+10H+,
故答案为:S2O32-+4Cl2+5H2O═2SO42-+8Cl-+10H+;
(2)发生氧化还原反应,生成锰离子、氧气、水,离子反应为5H2O2+2MnO4-+6H+=2Mn2++5O2↑+8H2O,故答案为:5H2O2+2MnO4-+6H+=2Mn2++5O2↑+8H2O;
(3)SO2通入硝酸铁溶液中,溶液由棕黄色变为浅绿色,铁离子与二氧化硫发生氧化还原反应生成硫酸根离子、亚铁离子,离子反应为SO2+2Fe3++2H2O=SO42-+2Fe2++4H+;立即又变为棕黄色,是因亚铁离子与硝酸根离子、氢离子发生氧化还原反应生成铁离子,离子反应为NO3-+3Fe2++4H+=3Fe3++NO↑+2H2O,
故答案为:SO2+2Fe3++2H2O=SO42-+2Fe2++4H+;NO3-+3Fe2++4H+=3Fe3++NO↑+2H2O;
(4)亚铁离子、溴离子均具有还原性,但亚铁离子还原性强,与等物质的量的氯气反应,亚铁离子全部被氧化,而溴离子一半被氧化,离子反应为2Fe2++2Br-+2Cl2═2Fe3++4Cl-+Br2,故答案为:2Fe2++2Br-+2Cl2═2Fe3++4Cl-+Br2.
故答案为:S2O32-+4Cl2+5H2O═2SO42-+8Cl-+10H+;
(2)发生氧化还原反应,生成锰离子、氧气、水,离子反应为5H2O2+2MnO4-+6H+=2Mn2++5O2↑+8H2O,故答案为:5H2O2+2MnO4-+6H+=2Mn2++5O2↑+8H2O;
(3)SO2通入硝酸铁溶液中,溶液由棕黄色变为浅绿色,铁离子与二氧化硫发生氧化还原反应生成硫酸根离子、亚铁离子,离子反应为SO2+2Fe3++2H2O=SO42-+2Fe2++4H+;立即又变为棕黄色,是因亚铁离子与硝酸根离子、氢离子发生氧化还原反应生成铁离子,离子反应为NO3-+3Fe2++4H+=3Fe3++NO↑+2H2O,
故答案为:SO2+2Fe3++2H2O=SO42-+2Fe2++4H+;NO3-+3Fe2++4H+=3Fe3++NO↑+2H2O;
(4)亚铁离子、溴离子均具有还原性,但亚铁离子还原性强,与等物质的量的氯气反应,亚铁离子全部被氧化,而溴离子一半被氧化,离子反应为2Fe2++2Br-+2Cl2═2Fe3++4Cl-+Br2,故答案为:2Fe2++2Br-+2Cl2═2Fe3++4Cl-+Br2.
点评:本题考查离子反应方程式的书写,为高频考点,把握发生的氧化还原反应及离子反应的书写方法为解答的关键,侧重氧化还原反应的离子方程式书写考查,(4)为解答的难点,题目难度不大.

练习册系列答案
相关题目
下列叙述中正确的是( )
①在标准状况下,0.2mol任何物质的体积均为4.48L
②当1mol气体的体积为22.4L时,它一定处于标准状况下
③标准状况下,1LHCl和1LH2O的物质的量相同
④标准状况下,1gH2和14gN2的体积相同
⑤28gCO的体积为22.4L
⑥同温同压下,气体的密度与气体的相对分子质量成正比.
①在标准状况下,0.2mol任何物质的体积均为4.48L
②当1mol气体的体积为22.4L时,它一定处于标准状况下
③标准状况下,1LHCl和1LH2O的物质的量相同
④标准状况下,1gH2和14gN2的体积相同
⑤28gCO的体积为22.4L
⑥同温同压下,气体的密度与气体的相对分子质量成正比.
| A、①②③④ | B、②③⑥ |
| C、⑤⑥ | D、④⑥ |
用NA表示阿伏加德罗常数的数值,下列说法正确的是( )
| A、标准状况下,22.4LH2O含有NA个分子 |
| B、1L1mol?L -1的NaClO 溶液中含有ClO-的数目少于NA个 |
| C、0.1molAlCl3完全转化为氢氧化铝胶体,生成0.lNA个胶体粒子 |
| D、0.1molCl2与足量NaOH溶液反应,转移电子数为0.2NA |
下列离子方程式中正确的是( )
| A、向Ba(OH)2溶液中滴加NaHSO4溶液至中性:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| B、三氯化铝溶液跟过量氨水反应:Al3++4NH3?H2O=AlO2-+4NH4++2H2O |
| C、向含1mol KAl(SO4)2的溶液中逐滴Ba(OH)2至生成沉淀的质量最大时的离子方程式:2Al3++3SO42-+3Ba2++6OH-=2 Al(OH)3↓+3BaSO4↓ |
| D、向澄清石灰水中加入几滴NaHCO3溶液:Ca2++OH-+HCO3-=CaCO3↓+H2O |
 材料的不断发展可以促进社会进步.
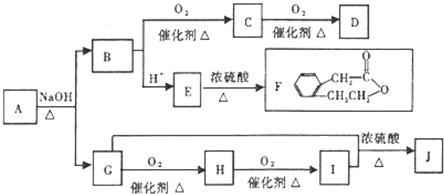
材料的不断发展可以促进社会进步.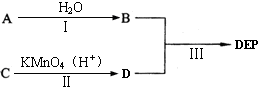 北京市疾病预防控制中心的调查结果显示,在北京市场上有九成受检香水和三成护发类化妆品被查出致癌物“邻苯二甲酸酯”(PAEs),值得注意的是,在儿童护肤类化妆品中亦有两件样品分别被检出邻苯二甲酸二乙酯(DEP)和邻苯二甲酸二(2-乙基己基)酯(DEHP).
北京市疾病预防控制中心的调查结果显示,在北京市场上有九成受检香水和三成护发类化妆品被查出致癌物“邻苯二甲酸酯”(PAEs),值得注意的是,在儿童护肤类化妆品中亦有两件样品分别被检出邻苯二甲酸二乙酯(DEP)和邻苯二甲酸二(2-乙基己基)酯(DEHP).