��Ŀ����
19�����ڿ��淴ӦN2+3H2?2NH3����Ӧ������ȥ�����ش��������⣺��1���ں��º��������£����б����У�����˵���÷�Ӧ�ﵽƽ��״̬����BD��
A����ϵ��ѹǿ���ֲ���
B��ijʱ��H2��NH3��Ũ��֮����3��2
C����ͬʱ���ڣ�����6NA��N-H����ͬʱ����3NA��H-H��
D��ijʱ�̷�Ӧ�������㣺3v��N2��=v��H2��
E����������ƽ��Ħ����������
��2�����д�ʩ�ܼӿ췴Ӧ���ʵ���C
A������ B����NH3�������ϵ C�����º��������£�����N2 D�����º�ѹ�����£�����He
��3������ôﵽƽ��ʱ��������������ת������ȣ���������������ʼͶ�����ʵ���֮��Ϊ1��3��
��4��������1mol N��N��Ҫ����akJ������1molH-H��Ҫ����bkJ���γ�1molN-H����ckJ�����n molN2�μӷ�Ӧ������N2��ȫת��������ù��̷���n��6c-a-3b��kJ��
��5���ں��º�ѹ���ܱ������У�����һ�����ĵ������������з�Ӧ�����ﵽƽ��ʱ�����������ܶ��Ƿ�Ӧǰ��1.2������ﵽƽ��ʱ����������а������������Ϊ20%��
���� ��1������Ӧ�ﵽƽ��״̬ʱ�����淴Ӧ������ȣ������ʵ�Ũ�ȡ��ٷֺ������䣬�Լ��ɴ�������һЩ��Ҳ�������仯��
��2������Ũ�ȡ������¶ȡ�����ѹǿ��ʹ�ô���������Ӧ��ĽӴ�����ܼӿ췴Ӧ���ʣ�
��3��ת����Ϊת��������ʼ���ı�ֵ��ת����������������ȣ�������������ת������ȣ�����ʼ���������Ҳ�����ȣ�
��4�����ѻ�ѧ�������������γɻ�ѧ���ų����������n molN2�μӷ�Ӧ�������2molN��N��3nmolH-H�����γ�6nmolN-H�����Դ˼��㷴Ӧ�ȣ�
��5����ѹ�����£���������仯���ﵽƽ��ʱ�����������ܶ��Ƿ�Ӧǰ��1.2���������Ϊԭ����$\frac{1}{1.2}$����ϲ��������㣮
��� �⣺��1��A����Ӧǰ�����������仯������ϵ��ѹǿ���ֲ��䣬��˵���ﵽƽ��״̬����A��ȷ��
B����ʼ���ϱ��Լ�ת���̶�δ֪��ijʱ��H2��NH3��Ũ��֮����3��2������ȷ���Ƿ�ﵽƽ��״̬����B����
C����ͬʱ���ڣ�����6NA��N-H����ͬʱ����3NA��H-H����˵�����淴Ӧ������ȣ��ﵽƽ��״̬����C��ȷ��
D����Ӧ����֮�ȵ��ڻ�ѧ������֮�ȣ�ijʱ�̷�Ӧ�������㣺3v��N2��=v��H2��������˵���ﵽƽ��״̬����D����
E����������ƽ��Ħ���������䣬��˵����������ʵ������䣬�ﵽƽ��״̬����E��ȷ��
�ʴ�Ϊ��BD��
��2��A�����£���Ӧ������ȣ���A����
B����NH3�������ϵ��Ũ�Ƚ��ͣ���Ӧ���ʼ�С����B����
C�����º��������£�����N2����Ӧ��Ũ������Ӧ��������C��ȷ��
D�����º�ѹ�����£�����He�����������Ũ�ȼ�С����Ӧ���ʼ�С����D����
�ʴ�Ϊ��C��
��3��ת����Ϊת��������ʼ���ı�ֵ��ת����������������ȣ�������������ת������ȣ�����ʼ���������Ҳ�����ȣ�ӦΪ1��3���ʴ�Ϊ��1��3��
��4�����ѻ�ѧ�������������γɻ�ѧ���ų����������n molN2�μӷ�Ӧ�������2molN��N��3nmolH-H�����γ�6nmolN-H������Ӧ�ų�������Ϊn��6c-a-3b��kJ��
�ʴ�Ϊ��n��6c-a-3b����
��5����ѹ�����£���������仯���ﵽƽ��ʱ�����������ܶ��Ƿ�Ӧǰ��1.2���������Ϊԭ����$\frac{1}{1.2}$���跴Ӧǰ���Ϊ1.2L����Ӧ��Ϊ1.0L��
N2����+3 H2��?2 NH3 ��V
1 3 2 2
0.2 1.2-1.0=0.2
�ﵽƽ��ʱ����������а������������Ϊ$\frac{0.2}{1.0}��100%$=20%��
�ʴ�Ϊ��20%��
���� ���⿼���Ϊ�ۺϣ��漰��ѧƽ��ļ��㣬ƽ��״̬���жϡ�ƽ���ƶ���Ӱ�������Լ���Ӧ�ȵļ�������⣬������ѧ���ķ��������ͼ��������Ŀ��飬ע����ռ����˼·�ͽǶȣ��ѶȲ���

 ��ĩ1�����ʽ���������ϵ�д�
��ĩ1�����ʽ���������ϵ�д�| A�� | ����������Һ��ϡ���ᷴӦ��H++OH-=H2O | |
| B�� | ����ϡ���ᷴӦ��2Fe+6H+=2Fe3++3H2�� | |
| C�� | ̼������Һ��ϡ���ᷴӦ��Na2CO3+2H+=2Na++H2O+CO2�� | |
| D�� | ����������Һ��ϡ���ᷴӦ��Ba2++SO42-=BaSO4�� |
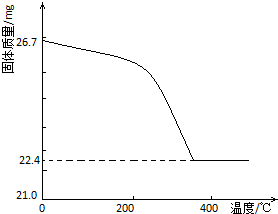 ��ҵ�ϴӷ�Ǧ���ص�Ǧ�����Ǧ�Ĺ����У�����̼������Һ��Ǧ�ࣨ��Ҫ�ɷ�ΪPbSO4��������Ӧ��PbSO4��s��+CO32-��aq��?PbCO3��s��+SO42-��aq����ij��������PbSO4Ϊԭ��ģ��ù��̣�̽��������Ӧ��ʵ���������������ijɷ֣�
��ҵ�ϴӷ�Ǧ���ص�Ǧ�����Ǧ�Ĺ����У�����̼������Һ��Ǧ�ࣨ��Ҫ�ɷ�ΪPbSO4��������Ӧ��PbSO4��s��+CO32-��aq��?PbCO3��s��+SO42-��aq����ij��������PbSO4Ϊԭ��ģ��ù��̣�̽��������Ӧ��ʵ���������������ijɷ֣���1��������Ӧ��ƽ�ⳣ������ʽ��K=$\frac{c��S{{O}_{4}}^{2-}��}{c��C{{O}_{3}}^{2-}��}$��
��2������ʱ����������ͬ����Ʒ�зֱ����ͬ�����ͬŨ�ȵ�Na2CO3��NaHCO3��Һ����ʵ������ת������Na2CO3��Һ��PbSO4ת���ʽϴ���������ͬŨ�ȵ�Na2CO3��NaHCO3��Һ�У�ǰ��c��CO32-���ϴ�
��3���������ף�������Ӧ���������ɼ�ʽ̼��Ǧ[2PbCO3•Pb��OH��2]������PbCO3���ȶ��ֽ�����PbO���ÿ�����Թ�����������PbSO4���ijɷ�������¼��裬������ɼ�����ͼ�������
����һ��ȫ��ΪPbCO3��
�������ȫ��Ϊ2PbCO3•Pb��OH��2��
��������PbCO3��2PbCO3•Pb��OH��2�Ļ���
��4��Ϊ��֤����һ�Ƿ��������������������о���
�ٶ����о�����������±������ݣ�
| ʵ�鲽�裨��Ҫ��д������������̣� | Ԥ�ڵ�ʵ������ͽ��� |
| ȡһ������Ʒ��ָ���� |
 �ȼ��仯�������������������й㷺����;���ش��������⣺
�ȼ��仯�������������������й㷺����;���ش��������⣺��1����������������ָ�ڼ����������ý���ˮ�е�CN-�����������ʣ�д���÷�Ӧ�����ӷ���ʽ��5Cl2+2CN-+8OH-�T10Cl-+N2��+2CO2��+4H2O
��2���ؿ����Ʊ������ķ�ӦΪ 4HCl��g��+O2��g��$\frac{\underline{\;CuO/CuCl\;}}{400��}$2Cl2��g��+2H2O��g����H=-115.6 kJ•mol-1��1 mol H-Cl��l mol Cl-Cl��1 mol O=O����ʱ�ֱ���Ҫ���� 431 KJ��243 kJ��489 kJ ���������� 1 mol OһH����ʱ�����յ�����Ϊ463.4kJ
��3��ȡClO2������������ˮ���ٶ�ClO2ȫ��ת��ΪCl-��30.00 mL��ˮ���м��˼���K2CrO4������Һ��ָʾ������һ��Ũ��AgNO3��Һ�ζ�������ש��ɫ��Ag2CrO4����������ʱ����Ӧ�ﵽ�ζ��յ㣮�����Һ
��CrO42-��Ũ����5.00��10-3 mol•L-1����ζ��յ�ʱ��Һ��c��Cl-��=8.90��10-6mol/L��[��֪��
KSP��AgCl��=1.78��10-10��Ksp��Ag2CrO4��=2.00��10-12]
��4����5�����¡������ܱ������зֱ����4 mol ClO2��������Ӧ4ClO2��g��?2Cl2O��g��+3O2��g����H��0�����ClO2��g���IJ���ƽ��ת���������ʾ��
| ������� | �¶�/�� | �������/L | Cl02��g����ƽ��ת���� |
| a | T1 | V1=l L | 75% |
| b | T1 | v2 | |
| c | T3 | v3 | 75% |
| d | |||
| e |
�ٸ÷�Ӧ��Cl2O�ǻ�ԭ������ԭ����������������
��T1��ʱ��������Ӧ��ƽ�ⳣ��K25.63
��V2�����������������=����V3
��d��e�������еķ�Ӧ��a�����еķ�Ӧ������һ��������ͬ��a��d��e�������з�Ӧ��ϵ��ѹǿ��ʱ��ı仯��ͼ��ʾ��a��d��e��������ClO2��ƽ��ת�����ɴ�С������˳��Ϊe��a=d������ĸ��ʾ������a������ȣ�d�����иı��һ��ʵ�������Ǽ�����������ж�������adͼ�������߱仯��֪��d��Ӧ��������ѹǿ����ƽ��㲻�䣮
| A�� | ������������ɢϵ��ʵ������Ƿ�ɢ�����ӵ�ֱ������1-100 nm֮�� | |
| B�� | �������Һ��һ���Ǿ�һ���ķ�ɢϵ�������ö����ЧӦ������ | |
| C�� | �Ʊ�Fe��OH��3����IJ���Ϊ���ڷ�ˮ����εμ�5��6��FeCl3������Һ�������������Һ�ʺ��ɫ������ֹͣ���� | |
| D�� | �ù��˵ķ������Խ��������Һ���� |
| A�� | Xһ��Ϊ����� | B�� | X����ΪNaCl | ||
| C�� | X���������� | D�� | X�������κλ����� |
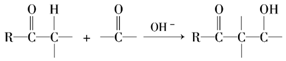 ��
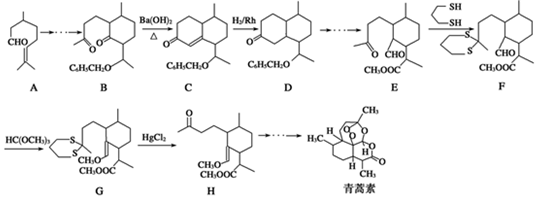
�� ���������մ��Ľṹ��ʽΪ
���������մ��Ľṹ��ʽΪ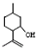 ��
��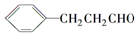 ���ĺϳ�·������ͼ�����Լ���ѡ����
���ĺϳ�·������ͼ�����Լ���ѡ����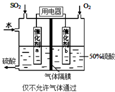 �ش��������⣺
�ش��������⣺ ��֪�Ȼ�ѧ����ʽH+��aq��+OH-��aq���TH2O��l����H=-57.3kJ/mol��
��֪�Ȼ�ѧ����ʽH+��aq��+OH-��aq���TH2O��l����H=-57.3kJ/mol��