题目内容
8.下列说法或表示方法中正确的是( )| A. | 若C(石墨,s)═C(金刚石,s)△H>0,则金刚石比石墨稳定 | |
| B. | 等质量的硫蒸气和硫磺固体分别完全燃烧,后者放出的热量多 | |
| C. | 相同体积浓度均为0.1 mol/L 盐酸和醋酸溶液分别与足量的NaOH稀溶液反应,前者放出热量多 | |
| D. | 氢气的燃烧热为285.8 kJ/mol,则氢气燃烧的热化学方程式为:2H2(g)+O2(g)═2H2O(l)△H=-285.8 kJ/mol |
分析 A.物质具有的能量越低越稳定;
B.硫蒸气变化为硫固体为放热过程;
C.醋酸是弱电解质,电离过程吸热;
D.燃烧热是1mol可燃物完全燃烧生成稳定氧化物时放出的热量.
解答 解:A.若C(石墨,s)═C(金刚石,s)△H>0,说明金刚石的能量比石墨高,因此石墨比金刚石稳定,故A错误;
B.硫蒸气变化为硫固体为放热过程,则等量的硫蒸气和硫固体在氧气中分别完全燃烧,前者放出热量多,故B错误;
C.醋酸是弱电解质,电离过程吸热,相同体积浓度均为0.1 mol/L 盐酸和醋酸溶液分别与足量的NaOH稀溶液反应,前者放出热量多,故C正确;
D.氢气的燃烧热为285.8 kJ/mol,则氢气燃烧的热化学方程式为:H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-285.8 kJ/mol,故D错误;
故选C.
点评 本题考查了化学反应能量变化,热化学方程式书写,燃烧热概念的理解应用,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
19.在25℃,101kPa下,0.1molC2H2完全燃烧生成CO2和H2O(I)时放出129.96kJ热量.表示上述反应的热化学方程式正确的是( )
| A. | 2C2H2(g)+5O2(g)→4CO2(g)+2H2O(l)+129.96kJ | |
| B. | 2C2H2(g)+5O2(g)→4CO2(g)+2H2O(g)-259.92kJ | |
| C. | 2C2H2(g)+5O2(g)→4CO2(g)+2H2O(l)-1299.6kJ | |
| D. | 2C2H2(g)+5O2(g)→4CO2(g)+2H2O(l)+2599.2kJ |
16.一氧化碳还原氧化铁:Fe2O3+3CO$\frac{\underline{\;\;△\;\;}}{\;}$2Fe+3CO2,在该反应中( )
| A. | 铁做还原剂 | B. | Fe2O3做氧化剂 | ||
| C. | 铁元素被还原 | D. | 铁元素化合价升高 |
13.下列各组物质的无色溶液,不用其它试剂即可鉴别的是( )
| A. | KOH Na2SO4 HCl | B. | NaHCO3 NaNO3 H2SO4 | ||
| C. | HCl Na2CO3 NaCl | D. | Ca(OH)2 Na2CO3 BaCl2 |
20.某铁的“氧化物”样品,用5mol/L的盐酸140mL恰好完全溶解,所得溶液还能吸收标准状况下0.56L氯气,使其中Fe2+全部转化为Fe3+.该样品可能的化学式是( )
| A. | Fe2O3 | B. | Fe3O4 | C. | Fe4O5 | D. | Fe5O7 |
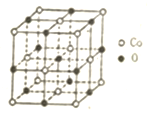 汽车安全气囊一般由传感器、气囊、气体发生器等组成.
汽车安全气囊一般由传感器、气囊、气体发生器等组成.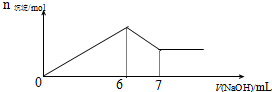 现有AlCl3和MgSO4混合溶液,向其中不断加入0.1mol/L 的NaOH溶液,得到沉淀的量与加入NaOH溶液的体积如图所示,原溶液中Cl-与SO42-的物质的量之比为( )
现有AlCl3和MgSO4混合溶液,向其中不断加入0.1mol/L 的NaOH溶液,得到沉淀的量与加入NaOH溶液的体积如图所示,原溶液中Cl-与SO42-的物质的量之比为( )