题目内容
5.下列说法中正确的是( )| A. | 分子式为C5H12的烷烃,含有3个甲基结构的同分异构体有2种 | |
| B. | 丙烯能发生加成反应,还能使酸性KMnO4溶液褪色 | |
| C. | 甲苯中所有原子都处于同一平面 | |
| D. | 相同质量的甲烷和乙烷完全燃烧,乙烷耗氧量多 |
分析 A.分子式为C5H12的烷烃,含有3个甲基结构的为2-甲基丁烷;
B.丙烯含有碳碳双键,可发生加成、氧化反应;
C.甲苯含有甲基,具有甲烷的结构特点;
D.根据含氢量判断,含氢量越高,耗氧量越大.
解答 解:A.分子式为C5H12的烷烃有正戊烷、新戊烷和异戊烷3种,含有3个甲基结构的为2-甲基丁烷,及异戊烷,只有一种,故A错误;
B.丙烯含有碳碳双键,可发生加成、氧化反应,则能发生加成反应,还能使酸性KMnO4溶液褪色,故B正确;
C.甲苯含有甲基,具有甲烷的结构特点,所有的原子不可能在同一个平面上,故C错误;
D.甲烷的含氢量较大,相同质量时消耗的氧气的量较多,故D错误.
故选B
点评 本题综合考查有机物的结构和性质,为高频考点,侧重于学生的分析能力的考查,此类题目注意把握物质的结构和官能团的性质,难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
15.为妥善处理氯甲烷生产企业的副产物CCl4,以减少其对臭氧层的破坏.化学家研究在催化条件下,通过下列反应,使CCl4转化为重要的化工原料氯仿(CHCl3).CCl4+H2?CHCl3+HCl
此反应伴随有副反应,会生成CH2Cl2、CH3Cl和CH4等.已知CCl4的沸点为77℃,CHCl3的沸点为61.2℃.
在密闭容器中,该反应达到平衡后,测得如下数据(假设不考虑副反应).
(1)此反应在110℃时平衡常数为1.
(2)实验l中,CCl4的转化率A大于50%(填“大于”、“小于”或“等于”).
(3)实验3中,B的值D(选填序号).
A.等于50% B.大于50% C.小于50%D.从本题资料,无法判断
(4)120℃,在相同条件的密闭容器中,分别进行H2的初始浓度为2mol•L-1和4mol•L-1的实验,测得反应消耗CCl4的百分率(x%)和生成物中CHCl3,的百分含量(y%)随时间(t)的变化关系如图(图中实线是消耗CCl4的百分率变化曲线,虚线是产物中CHCl3的百分含量变化曲线).在图中的四条线中,表示H2起始浓度为2mol•L-1实验的消耗CCl4的百分率变化曲线是c(选填序号).
此反应伴随有副反应,会生成CH2Cl2、CH3Cl和CH4等.已知CCl4的沸点为77℃,CHCl3的沸点为61.2℃.
在密闭容器中,该反应达到平衡后,测得如下数据(假设不考虑副反应).
| 实验 序号 | 温度℃ | 初始CCl4浓度 (mol•L-1) | 初始H2浓度(mol•L-1) | CCl4的平衡转化率 |
| 1 | 110 | 1 | 1.2 | A |
| 2 | 110 | 1 | 1 | 50% |
| 3 | 100 | 1 | 1 | B |
(2)实验l中,CCl4的转化率A大于50%(填“大于”、“小于”或“等于”).
(3)实验3中,B的值D(选填序号).
A.等于50% B.大于50% C.小于50%D.从本题资料,无法判断
(4)120℃,在相同条件的密闭容器中,分别进行H2的初始浓度为2mol•L-1和4mol•L-1的实验,测得反应消耗CCl4的百分率(x%)和生成物中CHCl3,的百分含量(y%)随时间(t)的变化关系如图(图中实线是消耗CCl4的百分率变化曲线,虚线是产物中CHCl3的百分含量变化曲线).在图中的四条线中,表示H2起始浓度为2mol•L-1实验的消耗CCl4的百分率变化曲线是c(选填序号).

16.在蒸发皿中加热蒸干下列物质的水溶液并灼烧固体,可以得到该溶质固体的是( )
| A. | 氯化铜 | B. | 碳酸氢钙 | C. | 高锰酸钾 | D. | 偏铝酸钠 |
13.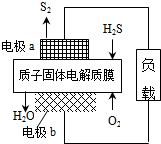 H2S废气资源化利用途径之一是回收能量并得到单质硫.反应原理为:2H2S(g)+O2(g)═S2(s)+2H2O(l)△H=-632kJ•mol-1.如图为质子膜H2S燃料电池的示意图.下列说法正确的是( )
H2S废气资源化利用途径之一是回收能量并得到单质硫.反应原理为:2H2S(g)+O2(g)═S2(s)+2H2O(l)△H=-632kJ•mol-1.如图为质子膜H2S燃料电池的示意图.下列说法正确的是( )
 H2S废气资源化利用途径之一是回收能量并得到单质硫.反应原理为:2H2S(g)+O2(g)═S2(s)+2H2O(l)△H=-632kJ•mol-1.如图为质子膜H2S燃料电池的示意图.下列说法正确的是( )
H2S废气资源化利用途径之一是回收能量并得到单质硫.反应原理为:2H2S(g)+O2(g)═S2(s)+2H2O(l)△H=-632kJ•mol-1.如图为质子膜H2S燃料电池的示意图.下列说法正确的是( )| A. | 电极a为电池的正极 | |
| B. | 电极b上发生的电极反应为:O2+2H2O+4e-=4 OH- | |
| C. | 电路中每流过4mol电子,电池内部释放632kJ热能 | |
| D. | 每17gH2S参与反应,有1mol H+经质子膜进入正极区 |
10.氯、溴、碘三种卤素单质的化学性质相似.其原因是( )
| A. | 颜色相似 | B. | 都是双原子分子 | ||
| C. | 最外层电子数相同,都是7 | D. | 自然界中都以化合态存在 |
17.下列溶液中NO3-的物质的量浓度最大的是( )
| A. | 500 mL 1 mol/L的HNO3溶液 | B. | 1 L 0.5 mol/L的Fe(NO3)3溶液 | ||
| C. | 100 mL 0.5 mol/L的Mg(NO3)2溶液 | D. | 300 mL 1 mol/L的Mg(NO3)2溶液 |
14.短周期主族元素X、Y、Z、W原子序数依次增大,X与Z原子序数相差8,Y元素的焰色为黄色,Z元素的最高价为+6.下列叙述正确的是( )
| A. | X2-的离子半径大于Y+的离子半径 | |
| B. | H2Z的沸点高于H2X | |
| C. | Z的简单气态氢化物稳定性比W的强 | |
| D. | Y2X2和Y2Z的晶体类型和化学键类型完全相同 |
15.NA表示阿伏加德罗常数,下列说法中正确的是( )
| A. | 1mol Na2O2中所含的离子数目为3NA | |
| B. | 标况下,22.4L氯气参与的反应中,转移的电子数一定为2NA | |
| C. | 0.1mol/L Al2(SO4)3溶液中,Al3+的数目为0.2NA | |
| D. | 1molSO2与足量O2在一定条件下反应生成SO3,共转移2NA个电子 |