题目内容
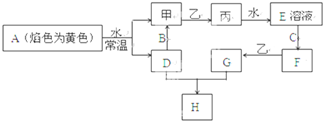
 A、B、C、D、E五种物质都含1~18号元素中的某一元素,它们按图所示关系相互转化,已知A为单质,D焰色反应为黄色火焰.
A、B、C、D、E五种物质都含1~18号元素中的某一元素,它们按图所示关系相互转化,已知A为单质,D焰色反应为黄色火焰.(1).写出化学式:
A.
(2).写出反应的化学方程式:
A→C:
(3).在A→D反应过程中,若生成标准状况下2240mL的H2,则转移的电子的物质的量为
考点:无机物的推断
专题:推断题
分析:A在氧气中燃烧生成C,A在空气中短期接触生成B,A与水反应生成D,且A、B、C都能和水反应生成D,A、C都是氧化物,都和水反应生成D,D只能为碱,A的元素为短周期元素,故A为Na,C为Na2O2,D为NaOH,E是Na2CO3,Na在空气中短期接触生成B,B为Na2O,Na2O与CO2反应生成Na2CO3,与水反应生成NaOH,符合转化关系,据此解答.
解答:
解:A在氧气中燃烧生成C,A在空气中短期接触生成B,A与水反应生成D,且A、B、C都能和水反应生成D,A、C都是氧化物,都和水反应生成D,D只能为碱,A的元素为短周期元素,故A为Na,C为Na2O2,D为NaOH,E是Na2CO3,Na在空气中短期接触生成B,B为Na2O,Na2O与CO2反应生成Na2CO3,与水反应生成NaOH,符合转化关系,
(1)由上述分析可知,A为Na,C为Na2O2,故答案为:Na;Na2O2;
(2)A→C是钠在空气中燃烧反应,反应方程式为:2Na+O2
Na2O2;
C→D是过氧化钠与水反应生成氢氧化钠与氧气,反应方程式为:2Na2O2+2H2O=4NaOH+O2↑;
A→D是钠与水反应生成氢氧化钠与氢气,反应方程式为:2Na+2H2O=2NaOH+H2↑,
故答案为:2Na+O2
Na2O2;2Na2O2+2H2O=4NaOH+O2↑;2Na+2H2O=2NaOH+H2↑;
(3)在钠与水的反应中根据方程式2Na+2H2O=2NaOH+H2↑,可知每产生1mol氢气转移2mol电子,所以生成标准状况下2240mL即0.1mol的H2,则转移的电子的物质的量为0.2mol,
故答案为:0.2mol.
(1)由上述分析可知,A为Na,C为Na2O2,故答案为:Na;Na2O2;
(2)A→C是钠在空气中燃烧反应,反应方程式为:2Na+O2
| ||
C→D是过氧化钠与水反应生成氢氧化钠与氧气,反应方程式为:2Na2O2+2H2O=4NaOH+O2↑;
A→D是钠与水反应生成氢氧化钠与氢气,反应方程式为:2Na+2H2O=2NaOH+H2↑,
故答案为:2Na+O2
| ||
(3)在钠与水的反应中根据方程式2Na+2H2O=2NaOH+H2↑,可知每产生1mol氢气转移2mol电子,所以生成标准状况下2240mL即0.1mol的H2,则转移的电子的物质的量为0.2mol,
故答案为:0.2mol.
点评:本题以无机框图题的形式考查Na元素单质及其化合物之间的相互转化关系、化学用语的书写等,比较基础,结合转化关系判断D为碱是关键,推断金属A为Na,然后进行验证.

练习册系列答案
相关题目
 用已知浓度的NaOH溶液测定某H2SO4溶液的浓度,参考如图所示从下表中选出正确选项( )
用已知浓度的NaOH溶液测定某H2SO4溶液的浓度,参考如图所示从下表中选出正确选项( )| 选项 | 锥形瓶中溶液 | 滴定管中溶液 | 选用指示剂 | 选用滴定管 |
| A | 碱 | 酸 | 石蕊 | 乙 |
| B | 酸 | 碱 | 酚酞 | 甲 |
| C | 碱 | 酸 | 甲基橙 | 乙 |
| D | 酸 | 碱 | 酚酞 | 乙 |
| A、A | B、B | C、C | D、D |
设NA代表阿伏伽德罗常数,下列说法中,正确的是( )
| A、17g NH3中所含的原子个数为3NA |
| B、22.4L氮气所含有的原子数为2NA |
| C、2.3g金属钠全部变成钠离子时失去的电子数目为0.2N |
| D、NA个氯气分子与NA氢气分子的质量比等于8:1 |
设NA为阿伏加德罗常数,下列有关叙述正确的是( )
| A、28g乙烯和28g丙烯分子中均含有6NA个共用电子对 |
| B、在熔融状态下,1molNaHSO4完全电离出的阳离子数目为2NA |
| C、7.8gNa2O2中含有阴离子数目为0.2NA |
| D、在含4molC=O键的干冰晶体中,碳原子的数目为4NA |
下列反应属于取代反应的是:①用甲烷和氯气反应制得氯仿;②在镍做催化剂的条件下,苯与氢气反应;③乙烯通入溴水中;④由乙烯制聚乙烯;⑤由甲苯制TNT;⑥乙烯使酸性高锰酸钾溶液褪色;⑦苯与液溴混合后撒入铁粉( )
| A、①③⑦ | B、⑤⑥⑦ |
| C、②③④ | D、①⑤⑦ |
 25℃,向20mL 0.1mol?L-1的醋酸溶液中不断滴入0.1mol?L-1的NaOH溶液,溶液pH的变化曲线如图,下列关于该过程中溶液中离子浓度大小关系的描述错误的是( )
25℃,向20mL 0.1mol?L-1的醋酸溶液中不断滴入0.1mol?L-1的NaOH溶液,溶液pH的变化曲线如图,下列关于该过程中溶液中离子浓度大小关系的描述错误的是( )| A、a点时:c( CH3COOH)>c( Na+)>c( CH3COO-)>c( H+)>c( OH-) |
| B、b点时:c( Na+)=c( CH3COO-)>c(H+)=c( OH-) |
| C、c点时:c(OH-)=c(CH3COOH)+c(H+) |
| D、d点时:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |