题目内容
已知:①2C(s)+O2(g)═2CO(g)△H=-221.0kJ?mol-1;②2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ?mol-1.则反应C(s)+H2O(g)═CO(g)+H2(g)的△H为( )
| A、+262.6 kJ?mol-1 |
| B、-131.3 kJ?mol-1 |
| C、-352.3 kJ?mol-1 |
| D、+131.3 kJ?mol-1 |
考点:用盖斯定律进行有关反应热的计算
专题:化学反应中的能量变化
分析:利用盖斯定律,
①-
②得到 C(s)+H2O(g)═CO(g)+H2(g)△H,反应热随之相加减,可求得反应热.
| 1 |
| 2 |
| 1 |
| 2 |
解答:
解:①2C(s)+O2(g)═2CO(g);△H=-221.0KJ/mol
②2H2(g)+O2(g)═2H2O;△H=-483.6KJ/mol
依据盖斯定律
①-
②得到 C(s)+H2O(g)═CO(g)+H2(g)
△H=
(-221.0+483.6)kJ/mol=+131.3kJ/mol;
故选D.
②2H2(g)+O2(g)═2H2O;△H=-483.6KJ/mol
依据盖斯定律
| 1 |
| 2 |
| 1 |
| 2 |
△H=
| 1 |
| 2 |
故选D.
点评:本题考查反应热的计算,为化学反应原理部分考试热点,题目难度不大,注意盖斯定律的运用.

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
同温同压下,等质量的下列气体所占有的体积最大的是( )
| A、O2 |
| B、CH4 |
| C、CO2 |
| D、SO2 |
从某些性质看,NH3与H2O、NH
与H3O+、NH
与OH-、NH2-与O2-相似,下列有关化学方程式不正确的是( )
+ 4 |
- 2 |
| A、氯化铵与KNH2反应:NH4Cl+KNH2═KCl+2NH3↑ |
| B、二价活泼金属M与液氨反应:M+2NH3═M(NH2)2+H2↑ |
| C、盐酸与MNH反应:2HCl+MNH═MCl2+NH3↑ |
| D、氯化铵与MO反应:2NH4Cl+MO═M(NH2)2+2HCl+H2O |
下列变化属于化学变化的是( )
| A、酒精挥发 | B、木料制成桌椅 |
| C、海水晒盐 | D、镁带燃烧 |
在25℃时,AgCl的白色悬浊液中,依次加入等浓度的KI溶液和Na2S溶液.观察到的现象是先出现黄色沉淀.最终出现黑色沉淀.已知有关物质的溶度积Ksp(25℃)如下:下列叙述错误的是( )
| AgCl | AgI | Ag2S | |
| Ksp | 1.8×10-10 | 8.51×10-16 | 6.3×10-50 |
| A、沉淀转化的实质就是沉淀溶解平衡的移动 |
| B、溶解度小的沉淀可以转化为溶解度更小的沉淀 |
| C、AgCl固体在等物质的量浓度的NaCl、CaCl2溶液中的溶解程度相同 |
| D、25℃时,在饱和AgCl、AgI、Ag2S溶液中,所含Ag+的浓度不同 |
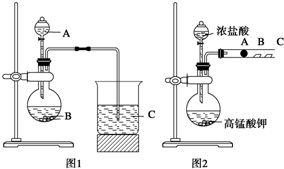 某研究性学习小组设计了一组实验来探究元素周期律.甲同学:根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成N、C、Si三种非金属元素的非金属性强弱比较的实验研究;
某研究性学习小组设计了一组实验来探究元素周期律.甲同学:根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成N、C、Si三种非金属元素的非金属性强弱比较的实验研究; 氨气的制取及性质探究(图中夹持装置均已略去).
氨气的制取及性质探究(图中夹持装置均已略去). 研究CO2的利用对促进低碳社会的构建具有重要的意义.
研究CO2的利用对促进低碳社会的构建具有重要的意义.