题目内容
下列说法正确的是( )
| A、标准状况下,1mol H2O和1mol H2的体积都约为22.4L |
| B、1molNa2CO3 中Na+ 的物质的量为1mol |
| C、1mol某气体的体积为22.4L |
| D、标准状况下,1g H2和 11.2LO2的物质的量相等 |
考点:物质的量的相关计算,气体摩尔体积
专题:
分析:A.标况下水不是气体,不能利用气体摩尔体积计算其体积;
B.钠离子物质的量为碳酸钠的2倍;
C.物质的量一定时,温度、压强会影响气体的体积;
D.根据n=
=
计算氢气、氧气物质的量,据此进行比较判断.
B.钠离子物质的量为碳酸钠的2倍;
C.物质的量一定时,温度、压强会影响气体的体积;
D.根据n=
| m |
| M |
| V |
| Vm |
解答:
解:A.标况下水不是气体,不能利用气体摩尔体积计算其体积,水的密度约是1g/mL,1mol水的体积远远小于22.4L,故A错误;
B.钠离子物质的量为1mol×2=2mol,故B错误;
C.标况下1mol气体的体积约是22.4L,但气体所处温度、压强不确定,物质的量一定时,温度、压强会影响气体的体积,不能确定其体积,故C错误;
D.1g氢气的物质的量为
=0.5mol,标况下11.2L氧气物质的量为
=0.5mol,二者物质的量相等,故D正确,
故选D.
B.钠离子物质的量为1mol×2=2mol,故B错误;
C.标况下1mol气体的体积约是22.4L,但气体所处温度、压强不确定,物质的量一定时,温度、压强会影响气体的体积,不能确定其体积,故C错误;
D.1g氢气的物质的量为
| 1g |
| 2g/mol |
| 11.2L |
| 22.4L/mol |
故选D.
点评:本题考查物质的量有关计算、气体摩尔体积,难度不大,注意气体摩尔体积的使用条件与对象,根据PV=nRT理解温度、压强对气体摩尔体积的影响.

练习册系列答案
相关题目
在一定温度下,CO和CH4燃烧的热化学方程式分别为:2CO(g)+O2(g)═2CO2(g)△H=-566kJ/mol
CH4(g)+O2(g)═
CO2(g)+H2O(l)△H=-445kJ/mol,1molCO和2mol CH4组成的混合气体,在相同条件下完全燃烧时,释放的热量为( )
| 1 |
| 2 |
| 1 |
| 2 |
| A、2346 kJ |
| B、2670 kJ |
| C、1698kJ |
| D、2063 kJ |
下列关于能量转换的认识中,不正确的是( )
| A、电解水生成氢气和氧气时,电能转化为化学能 |
| B、绿色植物进行光合作用时,太阳能转化为化学能 |
| C、每个化学反应都伴随着能量的变化 |
| D、当反应物浓度等于生成物浓度时,可逆反应一定已达到化学平衡状态 |
下列反应属于氧化还原反应的是( )
| A、14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4 | ||||
B、MgCl2(熔融)
| ||||
| C、CaCO3+2HCl═CaCl2+CO2↑+H2O | ||||
| D、Na2O+H2O═2NaOH |
设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A、常温常压下,23g的NO2含有的氧原子数为NA |
| B、已知某种元素的一种原子的质量为ag,则该元素的相对原子质量近似为aNA |
| C、某密闭容器盛有0.1molN2和0.4molH2,在一定条件下充分反应,转移电子的数目为0.6NA |
| D、80gNH4NO3晶体中含有NH4+小于NA个 |
某反应过程能量变化如图所示,下列说法正确的是( )
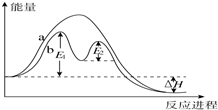

| A、反应过程a有催化剂参与 |
| B、该反应为放热反应,热效应不等于△H |
| C、使用催化剂,可改变该反应的活化能 |
| D、有催化剂条件下,反应的活化能等于E1-E2 |
下列化学反应的离子方程式正确的是( )
| A、往明矾溶液中逐滴加入氢氧化钡溶液至SO42-恰好完全沉淀Al3++2 SO42-+2 Ba2++4 OH-=2 BaSO4↓+AlO2-+2 H2O |
| B、少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-=CaSO3↓+2HClO |
| C、用稀HNO3溶液溶解FeS固体:FeS+2H+=Fe2++H2S↑ |
| D、AgNO3溶液中加入过量的氨水:Ag++NH3?H2O=AgOH↓+NH4+ |
 如图,水槽中试管内有一枚铁钉,放置数天观察,铁钉有明显生锈的迹象:
如图,水槽中试管内有一枚铁钉,放置数天观察,铁钉有明显生锈的迹象: