题目内容
8.周期表前20号元素中有A、B、C、D、E五种不同主族元素.已知它们原子半径依次增大,其中A与D、C与E原子的电子层数都相差2,且D与E原子的最外层电子数之比为2:1,C与E能形成离子化合物EC.(1)D元素的原子结构示意图为
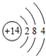 ;
;(2)B元素的名称为氟;
(3)用电子式表示A2C的形成过程
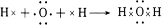 ;
;(4)写出E的碳酸氢盐与足量KOH溶液反应的离子方程式:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O;
(5)写出EA2与水反应放出气体的化学方程式,并用单线桥表示电子转移方向和数目
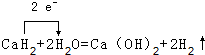 .
.
分析 周期表前20号元素中有A、B、C、D、E五种不同主族元素.已知它们原子半径依次增大,其中A与D、C与E原子的电子层数都相差2,D和E不能同时是第三周期的元素,否则A和C都是氢,结合原子半径知E是第四周期的元素中的钾或钙,D是第三周期的元素,A是氢,则E是钙(钾与氢同主族),D与E原子的最外层电子数之比为2:1,则D是硅,结合“C与E能形成离子化合物EC”知C是氧,根据原子半径知B是氟.
解答 解:周期表前20号元素中有A、B、C、D、E五种不同主族元素.已知它们原子半径依次增大,其中A与D、C与E原子的电子层数都相差2,D和E不能同时是第三周期的元素,否则A和C都是氢,结合原子半径知E是第四周期的元素中的钾或钙,D是第三周期的元素,A是氢,则E是钙(钾与氢同主族),D与E原子的最外层电子数之比为2:1,则D是硅,结合“C与E能形成离子化合物EC”知C是氧,根据原子半径知B是氟.
(1)D为Si元素,原子结构示意图为 ,故答案为:
,故答案为: ;
;
(2)B元素的名称为氟,故答案为:氟;
(3)用电子式表示H2O的形成过程: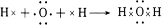 ,故答案为:
,故答案为: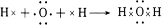 ;
;
(4)E的碳酸氢盐与足量KOH溶液反应的离子方程式:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O,故答案为:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O;
(5)CaH2与水反应放出气体,反应化学方程式:CaH2+2H2O=Ca(OH)2+2H2↑,并用单线桥表示电子转移方向和数目为: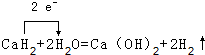 ,
,
故答案为: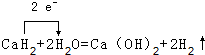 .
.
点评 本题考查结构性质位置关系应用,推断元素是解题关键,侧重考查学生的分析推理能力、常用化学用语等,(5)为易错点,中学基本不涉及金属氢化物,难度中等.

练习册系列答案
相关题目
18.短周期主族元素X、Y、Z、W的原子序数依次增大,X原子的最外层电子数是其内层电子数的2倍,Y和W同主族,Z+与Y2-具有相同的电子层结构.下列说法正确的是( )
| A. | 原子半径大小顺序:r(W)>r(Z)>r(Y)>r(X) | |
| B. | X的最高价氧化物对应水化物的酸性比W的弱 | |
| C. | Y分别与Z、W形成的化合物中化学键类型相同 | |
| D. | W的气态简单氢化物的热稳定性比Y的强 |
19.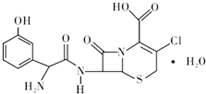 头孢克洛是人工合成的第二代口服头孢菌抗生素,主要用于上、下呼吸道感染、中耳炎、皮肤、尿道感染等症状,其结构如图所示,下列关于头孢克洛的说法错误的是( )
头孢克洛是人工合成的第二代口服头孢菌抗生素,主要用于上、下呼吸道感染、中耳炎、皮肤、尿道感染等症状,其结构如图所示,下列关于头孢克洛的说法错误的是( )
 头孢克洛是人工合成的第二代口服头孢菌抗生素,主要用于上、下呼吸道感染、中耳炎、皮肤、尿道感染等症状,其结构如图所示,下列关于头孢克洛的说法错误的是( )
头孢克洛是人工合成的第二代口服头孢菌抗生素,主要用于上、下呼吸道感染、中耳炎、皮肤、尿道感染等症状,其结构如图所示,下列关于头孢克洛的说法错误的是( )| A. | 其分子式可以表示为C15H16ClN3O6S | |
| B. | 该物质具有两性 | |
| C. | 1 mol该化合物与NaOH溶液作用时消耗NaOH的物质的量最多为 4 mol | |
| D. | 该物质遇FeCl3溶液显紫色 |
3.重铬酸钾(K2Cr2O7)是一种重要的无机试剂.
(1)①K2Cr2O7在加热条件下可以氧化浓盐酸产生氯气,其还原产物为Cr3+.该反应的离子方程式为Cr2O72-+14H++6Cl-$\frac{\underline{\;\;△\;\;}}{\;}$2Cr3++3Cl2↑+7H2O.
②常温下,Fe2+可将Cr2O72-还原为Cr3+,利用此反应原理可处理废水中有毒的Cr2O72-.某废水中Cr2O72-的浓度为0.005 mol/L,若处理10 L该废水至少需要绿矾(FeSO4•7H2O)83.4g.
(2)K2Cr2O7溶液中存在如下平衡:Cr2O72-(橙色)+H2O?2CrO42-(黄色)+2H+.
①若平衡体系的pH=2,则溶液显橙色.
②高温时,向饱和Na2Cr2O7溶液中先加入少量的硫酸,再加入一定量KCl固体,降温,就会析出K2Cr2O7晶体和NaCl晶体的混合物.加入少量硫酸的原因为H2SO4电离产生的H+使Cr2O72-+H2O?2CrO42-+2H+逆向移动,从而增大了c(Cr2O72-),提高K2Cr2O7产率;不同温度下,相关物质的溶解度数据如下表所示,请分析加入KCl固体后,降温会析出K2Cr2O7晶体的原因为K2Cr2O7的溶解度随温度降低减小的幅度大,使得复分解反应Na2Cr2O7+KCl=K2Cr2O7↓+NaCl得以发生,从而析出K2Cr2O7晶体.
③向K2Cr2O7溶液中加入Ba(NO3)2和Pb(NO3)2,可析出BaCrO4和PbCrO4两种沉淀,此时溶液中$\frac{c(P{b}^{2+})}{c(B{a}^{2+})}$=2.3×10-3.[已知:Ksp(BaCrO4)=1.2×10-10;Ksp(PbCrO4)=2.8×10-13].
(1)①K2Cr2O7在加热条件下可以氧化浓盐酸产生氯气,其还原产物为Cr3+.该反应的离子方程式为Cr2O72-+14H++6Cl-$\frac{\underline{\;\;△\;\;}}{\;}$2Cr3++3Cl2↑+7H2O.
②常温下,Fe2+可将Cr2O72-还原为Cr3+,利用此反应原理可处理废水中有毒的Cr2O72-.某废水中Cr2O72-的浓度为0.005 mol/L,若处理10 L该废水至少需要绿矾(FeSO4•7H2O)83.4g.
(2)K2Cr2O7溶液中存在如下平衡:Cr2O72-(橙色)+H2O?2CrO42-(黄色)+2H+.
①若平衡体系的pH=2,则溶液显橙色.
②高温时,向饱和Na2Cr2O7溶液中先加入少量的硫酸,再加入一定量KCl固体,降温,就会析出K2Cr2O7晶体和NaCl晶体的混合物.加入少量硫酸的原因为H2SO4电离产生的H+使Cr2O72-+H2O?2CrO42-+2H+逆向移动,从而增大了c(Cr2O72-),提高K2Cr2O7产率;不同温度下,相关物质的溶解度数据如下表所示,请分析加入KCl固体后,降温会析出K2Cr2O7晶体的原因为K2Cr2O7的溶解度随温度降低减小的幅度大,使得复分解反应Na2Cr2O7+KCl=K2Cr2O7↓+NaCl得以发生,从而析出K2Cr2O7晶体.
 | 20℃ | 60℃ | 100℃ |
| Na2Cr2O7 | 73.2 | 82.0 | 91.4 |
| K2Cr2O7 | 13.1 | 50.5 | 96.2 |
| NaCl | 36 | 37 | 39 |
| KCl | 34 | 45.5 | 56.7 |
13.反应4NH3(g)+5O2(g)?4NO(g)+6H2O(g)在5L密闭容器中进行,半分钟后NO的物质的量增加了0.3mol,则此反应的平均速率v为( )
| A. | v(O2)=0.01mol/(L•s) | B. | v(NO)=0.08mol/(L•s) | ||
| C. | v(H2O)=0.003mol/(L•s) | D. | v(NH3)=0.001mol/(L•s) |
17.下列有关绿色化学的叙述中,不正确的是( )
| A. | 绿色化学的核心是利用化学原理从源头上减少和消除工业生产对环境的污染 | |
| B. | 最理想的“原子经济”就是反应物的原子全部转化为期望的最终产物 | |
| C. | 绿色化学反应选择的原料、催化剂、溶剂都应该是无毒无害的 | |
| D. | 乙烯分别与溴水和溴的四氯化碳溶液反应制备1,2-二溴乙烷的原子利用率均为100% |
18. 伏打电堆(Voltaic pile)的照片和结构如图.它用圆形的锌板、铜板间隔堆积而成.所有的圆板之间夹放几层盐水泡过的布.下列说法正确的是( )
伏打电堆(Voltaic pile)的照片和结构如图.它用圆形的锌板、铜板间隔堆积而成.所有的圆板之间夹放几层盐水泡过的布.下列说法正确的是( )
 伏打电堆(Voltaic pile)的照片和结构如图.它用圆形的锌板、铜板间隔堆积而成.所有的圆板之间夹放几层盐水泡过的布.下列说法正确的是( )
伏打电堆(Voltaic pile)的照片和结构如图.它用圆形的锌板、铜板间隔堆积而成.所有的圆板之间夹放几层盐水泡过的布.下列说法正确的是( )| A. | 伏打电堆能将电能转化成化学能 | B. | 锌是正极 | ||
| C. | 盐水是电解质溶液 | D. | 伏打电堆工作时铜被还原 |
