题目内容
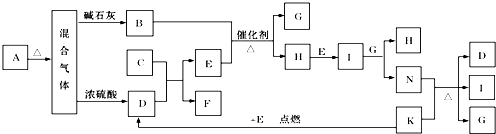
图中A~K分别代表有关反应的一种反应物或生成物,其中A、C、F、K是固体.已知A是一种不含金属元素的盐,受热分解得到三种产物物质的量之比为2:1:1;A加热后生成的混合气体若通过碱石灰,只剩余气体B(B为无色有刺激性气味的气体),若通过浓硫酸则只剩余气体D(D为无色无味气体);C为淡黄色固体.各物质间的转化关系如图所示:请回答:
(1)D中化学键的类型为 ,C的电子式 ,B的空间构型为 .
(2)写出A的溶液与足量NaOH溶液反应的离子方程式: .
(3)写出N与K反应的化学方程 .
(4)在标准状况下4.48L的H与I恰好被100mlNaOH溶液完全吸收,所需NaOH溶液的物质的量浓度为 mol?L-1.
(5)工业尾气中含有各种氮的氧化物(主要是NO和NO2,表示为NOx),NOx是严重的大气污染物,处理这些废气方法之一是通入适量的B,反应后会生成一种无色无味的气体.写出NOx与B反应的化学方程式: .

(1)D中化学键的类型为
(2)写出A的溶液与足量NaOH溶液反应的离子方程式:
(3)写出N与K反应的化学方程
(4)在标准状况下4.48L的H与I恰好被100mlNaOH溶液完全吸收,所需NaOH溶液的物质的量浓度为
(5)工业尾气中含有各种氮的氧化物(主要是NO和NO2,表示为NOx),NOx是严重的大气污染物,处理这些废气方法之一是通入适量的B,反应后会生成一种无色无味的气体.写出NOx与B反应的化学方程式:
考点:无机物的推断
专题:推断题
分析:A是一种不含金属元素的盐,应为铵盐,受热分解得到三种产物物质的量之比为2:1:1,A加热后生成的气体混合物若通过碱石灰,只剩余气体B(B为无色有刺激性气味的气体)推断为NH3,若通过浓硫酸则只剩余气体D,判断D为CO2,推断A为(NH4)2CO3,结合转化关系B+E在催化剂作用下加热生成G+H,H能发生连续反应,说明是氨气的催化氧化反应判断E为O2,G为H2O,H为NO,I为NO2,N为HNO3,D(CO2)+C=E(O2)+F,判断C为Na2O2,F为Na2CO3,依据转化关系K+E(O2)=D(CO2)反应是点燃条件下发生的反应,判断K为C,结合物质的性质及化学用语来解答.
解答:
解:A是一种不含金属元素的盐,应为铵盐,受热分解得到三种产物物质的量之比为2:1:1,A加热后生成的气体混合物若通过碱石灰,只剩余气体B(B为无色有刺激性气味的气体)推断为NH3,若通过浓硫酸则只剩余气体D,判断D为CO2,推断A为(NH4)2CO3,结合转化关系B+E在催化剂作用下加热生成G+H,H能发生连续反应,说明是氨气的催化氧化反应判断E为O2,G为H2O,H为NO,I为NO2,N为HNO3,D(CO2)+C=E(O2)+F,判断C为Na2O2,F为Na2CO3,依据转化关系K+E(O2)=D(CO2)反应是点燃条件下发生的反应,判断K为C,
(1)由以上分析可知D为CO2,含有极性共价键,C为Na2O2,电子式为 ,B为NH3,为三角锥形结构,
,B为NH3,为三角锥形结构,
故答案为:极性共价键; ;三角锥形;
;三角锥形;
(2)固体A为碳酸铵,溶液与足量NaOH溶液反应的离子方程式为NH4++OH-=NH3?H2O,故答案为:NH4++OH-=NH3?H2O;
(3)N与K反应的方程式为C+4HNO3
4NO2↑+CO2↑+2H2O,故答案为:C+4HNO3
4NO2↑+CO2↑+2H2O;
(4)在标准状况下4.48L的NO与NO2恰好被100mlNaOH溶液完全吸收,发生NO+NO2+2NaOH=2NaNO2+H2O,气体共为
=0.2mol,则n(NaOH)=0.2mol,
c(NaOH)=
=2mol/L,
故答案为:2;
(5)B为氨气,与NOx反应生成氮气和水,反应的方程式为6NOx+4xNH3=(2x+3)N2+6xH2O,故答案为:6NOx+4xNH3=(2x+3)N2+6xH2O.
(1)由以上分析可知D为CO2,含有极性共价键,C为Na2O2,电子式为
 ,B为NH3,为三角锥形结构,
,B为NH3,为三角锥形结构,故答案为:极性共价键;
 ;三角锥形;
;三角锥形;(2)固体A为碳酸铵,溶液与足量NaOH溶液反应的离子方程式为NH4++OH-=NH3?H2O,故答案为:NH4++OH-=NH3?H2O;
(3)N与K反应的方程式为C+4HNO3
| ||
| ||
(4)在标准状况下4.48L的NO与NO2恰好被100mlNaOH溶液完全吸收,发生NO+NO2+2NaOH=2NaNO2+H2O,气体共为
| 4.48L |
| 22.4L/mol |
c(NaOH)=
| 0.2mol |
| 0.1L |
故答案为:2;
(5)B为氨气,与NOx反应生成氮气和水,反应的方程式为6NOx+4xNH3=(2x+3)N2+6xH2O,故答案为:6NOx+4xNH3=(2x+3)N2+6xH2O.
点评:本题考查无机物的推断,注意元素化合物的性质应用,题目难度较大,本题解答时要善于抓住题中信息,为解答该题的关键,也是易错点,学习中要加强信息迁移能力的培养.

练习册系列答案
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案
相关题目
常温常压下,20mL某气态烃与85mL O2混合点燃并完全燃烧后恢复到原来状况,剩余气体为55mL,则此烃的化学式为( )
| A、C2H4 |
| B、C2H2 |
| C、C3H6 |
| D、C6H6 |
溴(Br)与氯同属“卤族”元素,其单质在性质上具有很大的相似性,但Cl2比Br2的活泼性强,下面是根据的氯性质对溴的性质的预测,其中不正确的是( )
| A、溴单质常温下为液态,但极容易挥发为溴蒸气 |
| B、溴单质只具有氧化性 |
| C、溴原子外层有7个电子,在化学反应中容易得1个电子,表现氧化性 |
| D、溴离子可以用酸性AgNO3溶液来检验 |