题目内容
请写出下列反应的化学方程式:
(1)乙炔与氢气用镍作催化剂在加热条件下发生加成反应生成乙烷.
(2)乙烯与水用硫酸作催化剂在加热条件下发生加成反应.
(3)1-丁烯与氢气用镍作催化剂在加热条件下发生加成反应.
(4)环已烷与溴的四氯化碳溶液在光照条件下反应生成一溴取代产物.
(1)乙炔与氢气用镍作催化剂在加热条件下发生加成反应生成乙烷.
(2)乙烯与水用硫酸作催化剂在加热条件下发生加成反应.
(3)1-丁烯与氢气用镍作催化剂在加热条件下发生加成反应.
(4)环已烷与溴的四氯化碳溶液在光照条件下反应生成一溴取代产物.
考点:化学方程式的书写
专题:
分析:(1)乙炔与氢气用镍作催化剂在加热条件下三键断裂发生加成反应生成乙烷;
(2)不饱和的C=C双键中其中1个C-C断裂结合水提供的-H、-OH,发生加成反应;
(3)1-丁烯与氢气用镍作催化剂在加热条件下生成丁烷;
(4)环己烷中只有一种位置的H,光照条件下反应生成一溴取代产物只有溴代环己烷.
(2)不饱和的C=C双键中其中1个C-C断裂结合水提供的-H、-OH,发生加成反应;
(3)1-丁烯与氢气用镍作催化剂在加热条件下生成丁烷;
(4)环己烷中只有一种位置的H,光照条件下反应生成一溴取代产物只有溴代环己烷.
解答:
解:(1)乙炔与氢气用镍作催化剂在加热条件下三键断裂发生加成反应生成乙烷,其方程式为:CH≡CH+2H2
CH3CH3,
故答案为:CH≡CH+2H2
CH3CH3;
(2)CH2=CH2中不饱和的C=C双键中其中1个C-C断裂结合水提供的-H、-OH,生成乙醇,方程式为:CH2=CH2+H2O
CH3CH2OH,
故答案为:CH2=CH2+H2O
CH3CH2OH;
(3)1-丁烯与氢气用镍作催化剂在加热条件下生成丁烷,其反应方程式为:CH2=CH-CH2CH3+H2
CH3CH2CH2CH3;
故答案为:CH2=CH-CH2CH3+H2
CH3CH2CH2CH3;
(4)环己烷与溴的四氯化碳溶液在光照条件下发生取代反应生成一溴环己烷和溴化氢,反应为 +Br2
+Br2
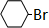 +HBr,
+HBr,
故答案为: +Br2
+Br2
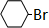 +HBr.
+HBr.
| Ni |
| △ |
故答案为:CH≡CH+2H2
| Ni |
| △ |
(2)CH2=CH2中不饱和的C=C双键中其中1个C-C断裂结合水提供的-H、-OH,生成乙醇,方程式为:CH2=CH2+H2O
| 浓H2SO4 |
| △ |
故答案为:CH2=CH2+H2O
| 浓H2SO4 |
| △ |
(3)1-丁烯与氢气用镍作催化剂在加热条件下生成丁烷,其反应方程式为:CH2=CH-CH2CH3+H2
| Ni |
| △ |
故答案为:CH2=CH-CH2CH3+H2
| Ni |
| △ |
(4)环己烷与溴的四氯化碳溶液在光照条件下发生取代反应生成一溴环己烷和溴化氢,反应为
 +Br2
+Br2| 光照 |
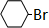 +HBr,
+HBr,故答案为:
 +Br2
+Br2| 光照 |
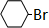 +HBr.
+HBr.
点评:本题考查有机物的结构与性质,把握官能团与性质的关系为解答的关键,侧重有机方程式书写的考查,题目难度不大.

练习册系列答案
相关题目
向盛有乙醇的烧杯中投入一小块金属钠,可以观察到的现象是( )
| A、钠块浮在乙醇液面上 |
| B、钠块熔成小球 |
| C、钠块与乙醇反应发出“嘶嘶”的声音 |
| D、钠块表面有气泡产生 |
设NA为阿伏伽德罗常数的值,则下列叙述错误的是( )
| A、1mol氧基(-OH)与16g氨基(-NH2)所含电子数为9NA |
| B、12.4白磷(分子式为P4,正四面体结构)中含有P-P共价键为0.6NA |
| C、标准状况下,11.2L氯仿(CHCl3)中含有C-Cl键的数目一定为1.5NA |
| D、7.1gCl2与5.6gFe充分燃烧反应,转移的电子总数一定为0.2NA |
(选做)T℃时,A气体与B气体反应生成C气体.反应过程中A、B、C浓度变化如图(Ⅰ)所示,若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如图(Ⅱ)所示,则下列结论正确的是( )


| A、在(t1+10)min时,保持其他条件不变,增大压强,平衡向逆反应方向移动 |
| B、(t1+10)min时,保持容器总压强不变,通入稀有气体,平衡向逆反应方向移动 |
| C、(t1+10)min时,保持容器体积不变,通入稀有气体,平衡向正反应方向移动 |
| D、其他条件不变,升高温度,正、逆反应速率均增大,且A的转化率增大 |
下列化学反应中,既是离子反应,又是氧化还原反应的是( )
| A、2NaOH+H2SO4═Na2SO4+2H2O | ||||
| B、Fe+H2SO4═FeSO4+H2↑ | ||||
| C、BaCl2+H2SO4═BaSO4↓+2HCl | ||||
D、H2+CuO
|
下列关于反应热和热化学反应的描述中正确的是( )
| A、HCl和NaOH反应的中和热△H=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)kJ/mol |
| B、CO的燃烧热是283.0kJ/mol,则2CO2(g)=2CO(g)+O2(g)反应的△H=+566.0kJ/mol |
| C、H2的燃烧热是285.5kJ/mol,则电解水的热化学方程式为:2H2O(l)=2H2(g)+O2(g)△H=+285.5kJ/mol |
| D、1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷燃烧热 |
Fe和Fe2O3、Fe3O4的混合物,加入200mL 5mol?L-1的盐酸,恰好完全溶解,再向其中加入KSCN溶液,未见血红色,则所得溶液中Fe2+的物质的量浓度为(假设反应后溶液体积仍为200mL)( )
| A、2.5mol?L-1 |
| B、lmol?L-1 |
| C、2mol?L-1 |
| D、5mol?L-1 |
 (也可表示为:
(也可表示为: )
)
 的流程图,写出由C合成D的流程图(无机试剂任选).
的流程图,写出由C合成D的流程图(无机试剂任选).