题目内容
标准状况下的甲烷和一氧化碳的混合气体8.96L,其质量为7.60g,求:
(1)混合气体的平均相对分子质量;
(2)混合气体中甲烷的体积;
(3)混合气体中一氧化碳的质量.
(1)混合气体的平均相对分子质量;
(2)混合气体中甲烷的体积;
(3)混合气体中一氧化碳的质量.
考点:气体摩尔体积,物质的量的相关计算
专题:十字交叉法
分析:由平均摩尔质量=
来计算,由质量和物质的量的关系列方程解出甲烷的物质的量,再计算混合气体中甲烷的体积和一氧化碳的质量.
| m |
| n |
解答:
解:(1)标准状况下,8.96L气体的物质的量为
=0.4mol,设甲烷的物质的量为x,CO的物质的量为y,
则
,解得x=0.3mol,y=0.1mol,
混合气体平均摩尔质量为
=19g/mol,
答:混合气体的相对分子质量为19;
(2)混合气体中甲烷的体积为0.3mol×22.4mol/L=6.72L,
答:甲烷的体积为6.72L;
(3)一氧化碳的质量为:0.1mol×28g/mol=2.8g,
答:一氧化碳的质量为2.8g.
| 8.96L |
| 22.4L/mol |
则
|
混合气体平均摩尔质量为
| 7.6g |
| 0.4mol |
答:混合气体的相对分子质量为19;
(2)混合气体中甲烷的体积为0.3mol×22.4mol/L=6.72L,
答:甲烷的体积为6.72L;
(3)一氧化碳的质量为:0.1mol×28g/mol=2.8g,
答:一氧化碳的质量为2.8g.
点评:本题主要考查的气体摩尔体积的有关计算,属于基础题.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
LiH是一种氢气发生剂,用于军事或其他需氢气的场合.反应为:LiH+H20═LiOH+H2↑在这个反应中( )
| A、水是氧化剂,LiH是还原剂 |
| B、LiH是氧化剂,水是还原剂 |
| C、LiH既是氧化剂又是还原剂 |
| D、该反应是非氧化还原反应,不存在氧化剂和还原剂 |
下列分散系最不稳定的是( )
| A、向CuSO4溶液中加入Ba(OH)2溶液得到的分散系 |
| B、向水中加入食盐得到的分散系 |
| C、向沸水中滴入饱和FeCl3溶液得到的红褐色液体 |
| D、向NaOH溶液中通入CO2得到的无色溶液 |
制备Fe(OH)3胶体的方法是( )
| A、氯化铁滴加到氢氧化钠溶液中 |
| B、氯化铁滴加到氢氧化钙溶液中 |
| C、氯化铁滴加到沸水中 |
| D、氯化铁滴加到沸水中,并搅拌 |
下列有关表述正确的是( )
A、次氯酸的电子式: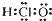 |
B、N原子的电子排布图: |
| C、硫原子的价电子排布式:3s23p4 |
| D、氯化钠的分子式:NaCl |
设NA 为阿伏加德罗常数的值.下列说法正确的是( )
| A、1 L 1 mol?L-1的NaClO 溶液中含有ClO-的数目为NA |
| B、标准状况下,0.1 mol Cl2 溶于水,转移的电子数目为0.1NA |
| C、常温常压下的33.6L氯气与27g铝充分反应,转移电子数为3NA |
| D、过氧化钠与水的反应中,每生成0.1mol氧气,转移电子的数目为0.2NA |
下列反应的离子方程式书写正确的是( )
| A、AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ |
| B、Cl2和H2O反应:Cl2+H2O═2H++Cl-+ClO- |
| C、盐酸与Na2SiO3溶液:SiO32-+2H+═H2SiO3↓ |
| D、铝粉投入到NaOH溶液中:2Al+2OH-═2AlO2-+H2↑ |


 一定条件下聚合生成一种合成纤维:
一定条件下聚合生成一种合成纤维: .
.