题目内容
6.以锌棒、铁棒、硫酸铜溶液组成原电池,正极上发生的反应为( )| A. | Fe═Fe2++2e- | B. | Cu2++2e-═Cu | C. | Fe═Fe3++3e- | D. | Zn═Zn2++2e- |
分析 活泼金属Zn易失电子作负极、铁作正极,正极上铜离子得电子生成铜单质,据此分析解答.
解答 解:以锌、铁为两极,硫酸铜溶液组成的原电池中,活泼金属Zn易失电子作负极、铁作正极,负极上锌失电子生成锌离子,正极上铜离子得电子生成铜单质,所以正极反应式为Cu2++2e-=Cu,故B正确,
故选B.
点评 本题考查电极反应式书写,为高频考点,明确各个电极上发生的反应是解本题关键,题目难度不大.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
17.下列说法中正确的是( )
| A. | 1mol•L-1的NaCl溶液是指由1mol NaCl和1000mL水配制成的溶液 | |
| B. | 从1L 0.5mol•L-1的NaCl溶液中取出100mL,剩余溶液物质的量浓度为0.45mol•L-1 | |
| C. | 标准状况下,18克H2O所含的氧原子数目为NA | |
| D. | 0℃时,2mol Cl2的体积不可能为22.4L |
6.在无色的酸性溶液中可以大量共存的离子组是( )
| A. | Fe2+ NO3- I-SO42- | B. | MnO4- K+NO3-Na+ | ||
| C. | K+Al3+Cl-SO42- | D. | Mg2+SO32-Br-Ba2+ |
7.下列有关实验操作的叙述,错误的是( )
| A. | 中和热的测定实验时,眼睛要注视温度计的刻度变化 | |
| B. | 萃取时,将混合物充分振荡后,需静置,待液体分层明显后才能分液 | |
| C. | 中和滴定实验时,为了使滴定终点的现象更加明显,可以滴加较多的指示剂 | |
| D. | 蒸馏时,温度计的读数刚达到某物质的沸点,不能立即收集馏出物 |
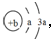 ,Y、Z为同周期金属元素,其中Y为短周期元素中原子半径最大的元素,Z为地壳中含量最高的金属元素,W的最高价氧化物对应水化物可以与其气态氢化物反应生成盐G,盐G溶液呈酸性,回答下列问题:
,Y、Z为同周期金属元素,其中Y为短周期元素中原子半径最大的元素,Z为地壳中含量最高的金属元素,W的最高价氧化物对应水化物可以与其气态氢化物反应生成盐G,盐G溶液呈酸性,回答下列问题: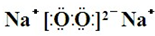 ,所含有的化学键类型为离子键和共价键.
,所含有的化学键类型为离子键和共价键.