题目内容
2.恒温下,将a mol N2与b mol H2的混合气体通入一个固定容积为2L的密闭容器中,发生如下反应:N2(g)+3H2(g)?2NH3(g)(1)若反应进行到5min时,nt(N2)=13mol,nt(NH3)=6mol,计算a=16
(2)用H2的浓度变化表示5min内的平均反应速率为0.9mol/(L•min);
(3)反应进行到10min时达平衡,混合气体的体积为716.8L(标况下),其中NH3的含量(体积分数)为25%.计算平衡时NH3的物质的量n(NH3)=8mol.
(4)原混合气体与平衡混合气体的总物质的量之比(写出最简整数比),n(始):n(平)=5:4.
分析 (1)恒温下,将a mol N2与b mol H2的混合气体通入一个固定容积的密闭容器中,若反应进行到某时刻t时,nt(N2)=13mol,nt(NH3)=6mol,则:
N2(g)+3H2(g)??2ΝΗ3(g)
起始量(mol):a b 0
变化量(mol):3 9 6
t时刻(mol):13 b-9 6
氮气起始物质的量=t时氮气物质的量+消耗氮气物质的量;
(2)反应速率v=$\frac{△c}{△t}$;
(3)根据n=$\frac{V}{{V}_{m}}$计算平衡时混合气体总物质的量,氨气物质的量=混合气体总物质的量×氨气体积分数;
(4)由(2)可知平衡时氨气物质的量,表示出平衡时各物质的物质的量,根据平衡时混合气体总物质的量计算b,恒温恒容下,压强之比等于物质的量之比.
解答 解:(1)恒温下,将a mol N2与b mol H2的混合气体通入一个固定容积的密闭容器中,若反应进行到某时刻t时,nt(N2)=13mol,nt(NH3)=6mol,则:
N2(g)+3H2(g)??2ΝΗ3(g)
起始量(mol):a b 0
变化量(mol):3 9 6
t时刻(mol):13 b-9 6
则a=3+13=16,
故答案为:16;
(2)用H2的浓度变化表示5min内的平均反应速率=$\frac{\frac{9mol}{2L}}{5min}$=0.9mol/(L•min),
故答案为:0.9mol/(L•min);
(3)平衡时混合气体物质的量为$\frac{716.8L}{22.4L/mol}$=32mol,氨气物质的量为32mol×25%=8mol,
故答案为:8mol;
(4)氨气物质的量为32mol×25%=8mol,则:
N2(g)+3H2(g)??2ΝΗ3(g)
起始量(mol):16 b 0
变化量(mol):4 12 8
平衡时(mol):12 b-12 8
则12+b-12+8=32,解得b=24,
恒温恒容下,压强之比等于物质的量之比,则P(始):P(平)=(16+24)mol:32mol=5:4,
故答案为:5:4.
点评 本题考查化学反应速率、化学平衡的计算,题目难度不大,注意三段式解题法在化学平衡计算中应用,掌握基础是解题关键.

 课堂练加测系列答案
课堂练加测系列答案 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案| A. | lmolC2H8N2中含有lmolN2 | |
| B. | 偏二甲肼的摩尔质量为60g | |
| C. | 偏二甲肼是比液氢更环保的燃料 | |
| D. | 偏二甲肼燃烧时能放出大量的热和气体 |
| A. | 该溶液一定呈酸性 | B. | 该溶液中的c(H+)可能等于10-3 | ||
| C. | 该溶液的pH可能为2,可能为12 | D. | 该溶液有可能呈中性 |
| A. | Fe═Fe2++2e- | B. | Cu2++2e-═Cu | C. | Fe═Fe3++3e- | D. | Zn═Zn2++2e- |
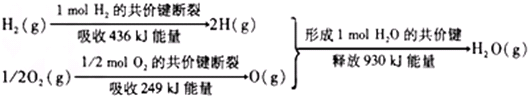
| A. | 氢气跟氧气反应生成水的同时释放能量 | |
| B. | 氢气跟氧气反应生成水的同时吸收能量 | |
| C. | 1 mol H2跟1/2 mol O2反应生成1 mol H2O释放能量不一定是245 kJ | |
| D. | 2 mol H2(g)跟1 mol O2(g)反应生成2 mol H2O(g)释放能量490 kJ |
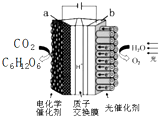 中关村“创客19”实验室模拟光合作用的电化学实验装置如右图所示,该装置能将H2O和CO2转化为O2和葡萄糖(C6H12O6).下列说法正确的是( )
中关村“创客19”实验室模拟光合作用的电化学实验装置如右图所示,该装置能将H2O和CO2转化为O2和葡萄糖(C6H12O6).下列说法正确的是( )| A. | 该装置是新型化学电源装置 | |
| B. | 该装置工作时,H+从a极区向b极区迁移 | |
| C. | 每生成1 mol O2,有44 g CO2被还原 | |
| D. | a 电极的反应为:6CO2+24H+-24e-=C6H12O6+6 H2 O |
| A. | Na+、Ba2+、Cl-、SO42- | B. | H+、NH4+、Al3+、SO42- | ||
| C. | H+、Fe2+、NO3-、Cu2+ | D. | K+、AlO2-、CH3COO-、NO3- |

| A. | 若A为浓盐酸,B为MnO2,C中盛品红溶液,则C中溶液褪色 | |
| B. | 若A为醋酸,B为碳酸钙,C中盛澄清石灰水,则C中溶液变浑浊 | |
| C. | 若A为浓氨水,B为生石灰,C中盛A1C13溶液,则C中先产生白色沉淀,后沉淀又溶解 | |
| D. | 若A为浓硫酸,B为Na2SO3固体,C中盛石蕊试液,则C中溶液先变红后褪色 |