题目内容
10.已知:2CO(g)+O2(g)═2CO2(g)△H=-566kJ•mol-1,下列说法正确的是( )| A. | CO的燃烧热为-283 kJ•mol-1 | |
| B. | CO的燃烧热为566 kJ•mol-1 | |
| C. | CO的燃烧热△H=-283 kJ•mol-1 | |
| D. |  如图可表示由CO生成CO2的反应过程和能量关系 |
分析 ABC、依据燃烧热是1mol可燃物完全燃烧生成稳定氧化物时放出热量;
D、依据热化学方程式,2CO(g)+O2(g)=2CO2(g)△H=-566kJ/mol分析图象中物质的量不符合反应物质物质的量.
解答 解:A、燃烧热是1mol可燃物完全燃烧生成稳定氧化物时放出热量;已知:2CO(g)+O2(g)=2CO2(g)△H=-566kJ/mol,一氧化碳的燃烧热为283kJ/mol,即△H=-283 kJ•mol-1,故AB错误,C正确;
D、热化学方程式,2CO(g)+O2(g)=2CO2(g)△H=-566kJ/mol,但图象中一氧化碳和氧气物质的量为1、$\frac{1}{2}$,物质的量不符合反应物质的物质的量,故D错误;
故选:C.
点评 本题考查了热化学方程式的计算应用,燃烧热概念计算分析,热化学方程式的书写方法和计算应用是解题关键,题目难度中等.

练习册系列答案
相关题目
20.下列有机化学反应方程式书写及反应类型均正确的是( )
| A. | CH2=CH2+HCl$\stackrel{催化剂}{→}$CH3CH2Cl 加聚反应 | |
| B. | CH3COOH+CH3CH2OH $?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH3+H2O 酯化反应 | |
| C. | 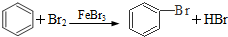 加成反应 加成反应 | |
| D. | 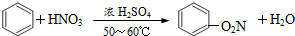 取代反应 取代反应 |
1.下列对聚丙烯酸酯不正确的说法是( )
| A. | 单体的结构简式为CH2═CHCOOR | B. | 在一定条件下能发生加成反应 | ||
| C. | 在一定条件下能发生水解反应 | D. | 没有固定熔沸点 |
18.在同温同压下,下列各组热化学方程式中,△H2>△H1的是( )
| A. | 2H2(g)+O2(g)=2H2O(g);△H12H2(g)+O2(g)=2H2O(l);△H2 | |
| B. | S(g)+O2(g)=SO2(g);△H1S(s)+O2(g)=SO2(g);△H2 | |
| C. | CO(g)+$\frac{1}{2}$O2(g)=CO2(g);△H12CO(g)+O2(g)=2CO2(g);△H2 | |
| D. | H2(g)+Cl2(g)=2HCl(g);△H1$\frac{1}{2}$H2(g)+$\frac{1}{2}$Cl2(g)=HCl(g);△H2 |
2.用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 含有NA个氮原子的氮气在标准状况下的体积约为11.2L | |
| B. | 25℃,1.01×105Pa,64g SO2中含有的原子数小于3NA | |
| C. | 在常温常压下,11.2LCl2含有的分子数为0.5NA | |
| D. | 标准状况下,11.2L H2O含有的分子数为0.5NA |
19.食品中可以按规定加入一定量的食品添加剂、干燥剂或除氧剂,下列说法正确的是( )
| A. | 补血营养品红桃K中添加微量铁粉,作为补铁剂 | |
| B. | 中秋月饼包装袋内有小袋铁粉,作为干燥剂 | |
| C. | 苏打饼干包装盒中有小袋生石灰,作为补钙剂 | |
| D. | 卤制品中加入大量亚硝酸钠,作为保鲜剂 |
20.设NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 14g C2H4和C3H6的混合物中,所含原子的总数为3NA | |
| B. | 足量的Fe与2.24 L Cl2反应转移的电子数为0.2NA | |
| C. | 0.1 mol•L-1的MgCl2溶液中含Cl-的数目为0.2NA | |
| D. | 1.8g H218O中所含中子数为NA |