题目内容
9.如图装置或操作不合理或不能达到实验目的是( )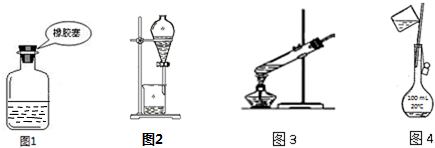
| A. | 图1装置:存放NaOH溶液 | |
| B. | 图2装置:分离乙酸乙酯和水 | |
| C. | 图3装置:葡萄糖的银镜反应 | |
| D. | 图4装置:配制 100 mL 1 mol/L NaCl溶液 |
分析 A.氢氧化钠与玻璃中的二氧化硅反应生成具有黏性的硅酸钠;
B.乙酸乙酯和水不溶;
C.银镜反应应用水浴加热;
D.容量瓶只有一个刻度.
解答 解:A.氢氧化钠与玻璃中的二氧化硅反应生成具有黏性的硅酸钠,易导致玻璃塞打不开,应用橡皮塞,故A正确;
B.乙酸乙酯和水不溶,可用分液分离,故B正确;
C.银镜反应应用水浴加热,不能直接加热,故C错误;
D.容量瓶只有一个刻度,100mL容量瓶可配制 100 mL 1 mol/L NaCl溶液,故D正确.
故选C.
点评 本题考查化学实验方案的评价,涉及物质的制备、保存、溶液配制以及乙酸乙酯的制备等知识,侧重于学生的分析能力、实验能力和评价能力的考查,为高考常见题型和高频考点,注意把握物质的性质的异同以及实验的严密性和合理性,难度不大.

练习册系列答案
相关题目
16.下列说法正确的是( )
| A. | SO2、CaO、CO均为酸性氧化物 | |
| B. | 硫酸钡和水都是弱电解质 | |
| C. | 向煮沸的1mol•L-1 NaOH溶液中滴加饱和FeCl3溶液制备Fe(OH)3胶体 | |
| D. | 福尔马林、水玻璃、氨水均为混合物 |
20.在体积一定的密闭容器中进行如下反应:A2(g)+2B2(g)?2C(g),已知A2、B2、C的起始浓度分别为a mol/L、b mol/L、0.3mol/L(非平衡态),在一定条件下,当反应达到平衡时,C的浓度为 0.5mol/L,则下列判断正确的是( )
| A. | 达平衡时,A2的正反应速率与B2的逆反应速率相等 | |
| B. | b≤0.2mol/L | |
| C. | 其它条件不变,在反应过程中使用了催化剂,可提高 A2、B2的转化率 | |
| D. | 该反应达平衡时气体物质的量浓度之和小于(a+b+0.3)mol/L |
17.下列各组物质中,化学键类型完全相同的是( )
| A. | MgBr2和KCl | B. | Cl2和HCl | C. | HI和NaI | D. | Na2O2和H2O2 |
4.在恒温恒容容器中,当下列哪些物理量不再发生变化时,表明反应A(g)+2B(g)?C(g)+D(g)已达到平衡状态( )
①混合气体的压强 ②混合气体的密度 ③B的物质的量浓度 ④混合气体的总物质的量 ⑤混合气体的平均相对分子质量 ⑥v(C)与v(D)的比值 ⑦混合气体的总质量⑧混合气体的总体积.
①混合气体的压强 ②混合气体的密度 ③B的物质的量浓度 ④混合气体的总物质的量 ⑤混合气体的平均相对分子质量 ⑥v(C)与v(D)的比值 ⑦混合气体的总质量⑧混合气体的总体积.
| A. | ①③④⑤ | B. | ①②③④⑤⑦ | C. | ①③④⑤⑧ | D. | ①②③④⑤⑥⑦⑧ |
18.已知同周期两种非金属元素X、Y,电负性X>Y,下列说法错误的是( )
| A. | 含氧酸的酸性:X对应的强于Y对应的 | |
| B. | 气态氢化物的稳定性:HmX强于HnY | |
| C. | 第一电离能可能Y大于X | |
| D. | X与Y形成化合物时,X显负价,Y显正价 |

 .CaC2晶胞结构与氯化钠晶体相似,则在晶体中与钙离子距离最近的C22-数目为6,这些C22-在空间所围成的几何图形为正八面体
.CaC2晶胞结构与氯化钠晶体相似,则在晶体中与钙离子距离最近的C22-数目为6,这些C22-在空间所围成的几何图形为正八面体 已知A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大.其中A原子所处的周期数、族序数都与其原子序数相等.B和C属同一主族,D和E属同一周期,又知E是周期表中1-18 列中的第7列元素.D的原子序数比E小5,D跟B可形成离化合物其晶胞结构如图.
已知A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大.其中A原子所处的周期数、族序数都与其原子序数相等.B和C属同一主族,D和E属同一周期,又知E是周期表中1-18 列中的第7列元素.D的原子序数比E小5,D跟B可形成离化合物其晶胞结构如图.