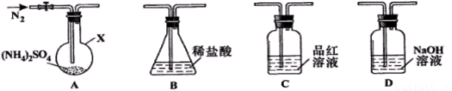
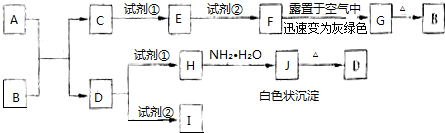
题目内容
2.一定温度下,在容积固定的密闭容器中,反应2SO2(g)+O2(g)?2SO3(g)达到平衡后,再通人气体18O2,重新达到平衡,下列说法不正确的是( )| A. | 平衡向正反应方向移动 | |
| B. | 前后两次平衡后,容器内的压强不相等次是相等 | |
| C. | SO2、O2的转化率均增大 | |
| D. | 通18O2前、通18O2后、重新到平衡后三个时间段,v(正)与v(逆)的关系依次是相等、大于、相等 |
分析 A、增大反应浓度,平衡向正反应方向移动;
B、通人气体18O2,增大反应浓度,气体压强增大,达到平衡后,容器内的压强比之前增大;
C、增加18O2浓度,SO2转化率增大,O2本身的转化率减小;
D、平衡时,v(正)=v(逆),通18O2后、正反应速率增大,v(正)>v(逆).
解答 解:A、增大反应浓度,平衡向正反应方向移动,故A正确;
B、通人气体18O2,增大反应浓度,气体压强增大,达到平衡后,容器内的压强比之前增大,故B正确;
C、增加18O2浓度,SO2转化率增大,O2本身的转化率减小,故C错误;
D、通18O2前,已经平衡,v(正)=v(逆),通18O2后、正反应速率增大,v(正)>v(逆),重新到平衡后,v(正)=v(逆),故D正确;
故选C.
点评 本题主要考查了影响化学反应速率的因素以及影响化学平衡移动的因素和转化率相关知识,难度不大.

练习册系列答案
相关题目
13.从经济效益和环境保护考虑,大量制取Cu(NO3)2最宜采用的方法是( )
| A. | Cu $\stackrel{浓HNO_{3}}{→}$Cu(NO3)2 | |
| B. | Cu$\stackrel{稀HNO_{3}}{→}$Cu(NO3)2 | |
| C. | Cu$→_{△}^{O_{2}(空气)}$ CuO$→_{△}^{稀HNO_{3}}$Cu(NO3)2 | |
| D. | Cu$→_{△}^{Cl_{2}}$CuCl2$\stackrel{AgNO_{3}溶液}{→}$ Cu(NO3)2 |
7.已知某溶液中存在较多的H+、SO42-、NO3-,则该溶液中还可能大量存在的离子组是( )
| A. | Al3+、CH3COO-、Cl- | B. | Mg2+、Ba2+、Br- | ||
| C. | Mg2+、Cl-、I- | D. | Na+、NH4+、Cu2+ |
14.第ⅢA族R元素在地壳中的丰度约为0.001%,单质熔点2180℃,原子半径小于铍,则关于R的叙述不正确的是( )
| A. | 是非金属元素 | B. | 单质是分子晶体 | ||
| C. | R(OH)4-结合H+的能力小于Al(OH)4- | D. | R2H6中R为-3价 |
2.关于晶体的下列说法正确的是( )
| A. | 任何晶体中,若含有阳离子就一定有阴离子 | |
| B. | 原子晶体中只含有共价键 | |
| C. | 原子晶体的熔点一定比金属晶体的高 | |
| D. | 分子晶体中只含有范德华力 |
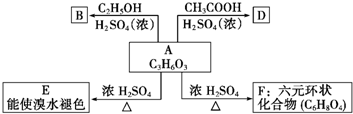
 .
.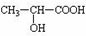 +CH3CH2OH $→_{△}^{浓硫酸}$
+CH3CH2OH $→_{△}^{浓硫酸}$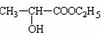 +H2O,
+H2O,