题目内容
19.在0.2molAl2(SO4)3中含有Al3+的数目是( )| A. | 2.408×1023 | B. | 3.612×1023 | C. | 0.4 | D. | 0.6 |
分析 先计算出0.2molAl2(SO4)3中含有的铝离子的物质的量,然后根据N=nNA计算出含有铝离子的数目.
解答 解:0.2molAl2(SO4)3中局铝离子的物质的量为:0.2mol×2=0.4mol,含有Al3+的数目为:0.4mol×6.02×1023mol-1=2.408×1023,
故选A.
点评 本题考查了物质的量的计算,题目难度不大,明确物质的量与阿伏伽德罗常数之间的关系即可解答,试题侧重基础知识的考查,培养了学生的化学计算能力.

练习册系列答案
相关题目
11.某气体体积为4.48L,质量为6.4g,含有6.02×1022个分子,则该气体的相对分子质量是( )
| A. | 32 | B. | 64 | C. | 96 | D. | 124 |
10.室温下,将amol钠和amol铝一同放入mg水(足量)中,所得溶液的密度为dg/mL,下列说法正确的是( )
| A. | 该溶液的物质的量浓度:$\frac{ad}{46a+m}$mol/L | |
| B. | 所得气体体积为44.8aL | |
| C. | 向溶液中通入过量CO2,未见白色沉淀 | |
| D. | 该溶液的质量分数:$\frac{8200a}{46a+m}$% |
14.下列离子方程式的书写正确的是( )
| A. | 少量NaHCO3溶液与Ca(OH)2溶液反应:OH-+HCO3-=CO32-+H2O | |
| B. | 向AlCl3溶液中加入过量NaOH溶液:Al3++3OH-=Al(OH)3↓ | |
| C. | 实验室用NH4Cl和Ca(OH)2共热制取NH3:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| D. | CO2和足量澄清石灰水反应:CO2+Ca2++2OH-=CaCO3↓+H2O |
4.某溶液中含有大量的Cl-、CO32-两种阴离子,如果只取一次该溶液就能够分别将两种阴离子检验出来,下列实验操作顺序正确的是( )
①过滤;②滴加AgNO3溶液;③滴加过量Ba(NO3)2溶液.
①过滤;②滴加AgNO3溶液;③滴加过量Ba(NO3)2溶液.
| A. | ①②③ | B. | ②①③ | C. | ③②① | D. | ③①② |
11.用NA表示阿伏加德罗常数的值,下列叙述中确的是( )
| A. | 7gCnH2n中含有的氢原子数目为NA | |
| B. | 标准状况下,22.4LCHCl3中含原子总数等于5NA | |
| C. | 1molC5H12分子中所含单键数为15NA | |
| D. | 标准状况下,11.2L已烷中含3mol碳原子 |
2.已知金属钠的活泼性非常强,甚至在常温时能和水发生反应2Na+2H2O═2NaOH+H2↑.现将9.2克钠、7.2克镁、8.1克铝分别放入100克10.95%的盐酸中,同温同压下产生气体的质量比是( )
| A. | 1:2:3 | B. | 4:3:3 | C. | 8:6:9 | D. | 1:1:1 |
 ,为了研究X的结构,将化合物A在一定条件下水解只得到B(分子式为C8H8O3)和C(分子式为C7H6O3).C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生.
,为了研究X的结构,将化合物A在一定条件下水解只得到B(分子式为C8H8O3)和C(分子式为C7H6O3).C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生.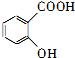 .
. .
. 为主要原料制备
为主要原料制备 的合成路线流程图(无机试剂任选).
的合成路线流程图(无机试剂任选).

