题目内容
(1)向MnSO4和硫酸的混合溶液里加入K2S208(过二硫酸钾),溶液中会发生如下反应:
Mn2++S2082-+H2O→MnO4-+SO42-+H+该反应常用于检验Mn2+的存在.其特征现象是 .
若反应中有0.1mol还原剂参加反应,则消耗氧化剂的物质的量为 mol.
(2)若该反应所用的硫酸锰改为氯化锰,当它跟过量的过硫酸钾反应时,除有高锰酸钾、硫酸钾、硫酸生成外,其他的生成物还有 .
(3)将NaBiO3固体(黄色微溶)加入到MnSO3和H2S04的混合溶液里加热,固体溶解变为澄清溶液,发生如下反应:
NaBi03+ MnSO4+ H2S04→ Na2S04+ Bi2(S04)3+ NaMnO4+ H2O
①配平上述反应的化学方程式;
②上述反应中还原产物是 .
③用单线桥表示该氧化还原反应
(4)S2O82-在一定条件下,可转变为S2O32-,写出往K2S2O3中滴加稀硫酸的离子方程式: .
Mn2++S2082-+H2O→MnO4-+SO42-+H+该反应常用于检验Mn2+的存在.其特征现象是
若反应中有0.1mol还原剂参加反应,则消耗氧化剂的物质的量为
(2)若该反应所用的硫酸锰改为氯化锰,当它跟过量的过硫酸钾反应时,除有高锰酸钾、硫酸钾、硫酸生成外,其他的生成物还有
(3)将NaBiO3固体(黄色微溶)加入到MnSO3和H2S04的混合溶液里加热,固体溶解变为澄清溶液,发生如下反应:
①配平上述反应的化学方程式;
②上述反应中还原产物是
③用单线桥表示该氧化还原反应
(4)S2O82-在一定条件下,可转变为S2O32-,写出往K2S2O3中滴加稀硫酸的离子方程式:
考点:氧化还原反应
专题:氧化还原反应专题
分析:(1)MnO4-为紫色,其它离子均为无色;Mn元素的化合价升高,S元素的化合价降低,利用电子守恒计算;
(2)硫酸锰改为氯化锰,当它跟过量的过硫酸钾反应时,氯离子可能被氧化;
(3)Bi元素的化合价由+5价降低为+3价,Mn元素的化合价由+2价升高为+7价,结合电子守恒、原子守恒分析;
(4)K2S2O3中滴加稀硫酸,发生氧化还原反应生成硫酸钾、S、二氧化硫和水.
(2)硫酸锰改为氯化锰,当它跟过量的过硫酸钾反应时,氯离子可能被氧化;
(3)Bi元素的化合价由+5价降低为+3价,Mn元素的化合价由+2价升高为+7价,结合电子守恒、原子守恒分析;
(4)K2S2O3中滴加稀硫酸,发生氧化还原反应生成硫酸钾、S、二氧化硫和水.
解答:
解:(1)MnO4-为紫色,其它离子均为无色,则反应的现象为溶液由无色变为紫色;Mn元素的化合价升高,S元素的化合价降低,有0.1mol还原剂(MnSO4)参加反应,则消耗氧化剂的物质的量为
=0.25mol,故答案为:溶液由无色变为紫色;0.25;
(2)硫酸锰改为氯化锰,当它跟过量的过硫酸钾反应时,氯离子可能被氧化,则除有高锰酸钾、硫酸钾、硫酸生成外,其他的生成物还有Cl2,故答案为:Cl2;
(3)①Bi元素的化合价由+5价降低为+3价,Mn元素的化合价由+2价升高为+7价,结合电子守恒、原子守恒可知,反应为10NaBi03+4MnSO4+14H2S04=3Na2S04+5Bi2(S04)3+4NaMnO4+14H2O,故答案为:10;4;14;3;5;4;14;
②Bi元素的化合价降低,被还原,对应还原产物为Bi2(SO4)3,故答案为:Bi2(SO4)3;
③Mn失去电子,Bi得到电子,该反应中转移20e-,用单线桥表示该氧化还原反应为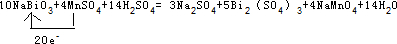 ,
,
故答案为: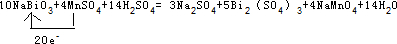 ;
;
(4)K2S2O3中滴加稀硫酸,发生氧化还原反应生成硫酸钾、S、二氧化硫和水,离子反应为S2O32-+2H+=S↓+SO2↑+H2O,故答案为:S2O32-+2H+=S↓+SO2↑+H2O.
| 0.1mol×(7-2) |
| 2×(7-6) |
(2)硫酸锰改为氯化锰,当它跟过量的过硫酸钾反应时,氯离子可能被氧化,则除有高锰酸钾、硫酸钾、硫酸生成外,其他的生成物还有Cl2,故答案为:Cl2;
(3)①Bi元素的化合价由+5价降低为+3价,Mn元素的化合价由+2价升高为+7价,结合电子守恒、原子守恒可知,反应为10NaBi03+4MnSO4+14H2S04=3Na2S04+5Bi2(S04)3+4NaMnO4+14H2O,故答案为:10;4;14;3;5;4;14;
②Bi元素的化合价降低,被还原,对应还原产物为Bi2(SO4)3,故答案为:Bi2(SO4)3;
③Mn失去电子,Bi得到电子,该反应中转移20e-,用单线桥表示该氧化还原反应为
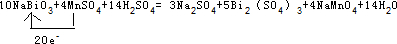 ,
,故答案为:
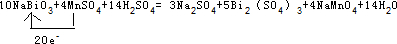 ;
;(4)K2S2O3中滴加稀硫酸,发生氧化还原反应生成硫酸钾、S、二氧化硫和水,离子反应为S2O32-+2H+=S↓+SO2↑+H2O,故答案为:S2O32-+2H+=S↓+SO2↑+H2O.
点评:本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念、转移电子及配平的考查,综合性较强,题目难度不大.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
提纯含有少量硝酸钡杂质的硝酸钾溶液,设计实验方案为
 则X试剂为( )
则X试剂为( )
 则X试剂为( )
则X试剂为( )| A、Na2CO3 |
| B、K2CO3 |
| C、Na2SO4 |
| D、K2SO4 |
下列说法正确的是( )
| A、淀粉和纤维素的最终水解产物都是葡萄糖,二者互为同分异构体 |
| B、石油经过分馏及裂化等工序得到的物质均为纯净物 |
| C、苯和甲苯互为同系物,均能使KMnO4酸性溶液褪色 |
D、结构片段 的高聚物,其单体是苯酚和甲醛 的高聚物,其单体是苯酚和甲醛 |
下列反应中,属于取代反应的是( )
①CH3CH=CH2+Br2
CH3CHBrCH2Br
②CH3CH2OH
CH2=CH2+H2O
③CH3COOH+CH3CH2OH
CH3COOCH2CH3+H2O
④2CH3CH2OH
CH3CH2OCH2CH3+H2O.
①CH3CH=CH2+Br2
| ccl4 |
②CH3CH2OH
| 浓H2So4 |
| △ |
③CH3COOH+CH3CH2OH
| 浓H2SO4 |
| △ |
④2CH3CH2OH
| 浓H2SO4 |
| △ |
| A、①② | B、③④ | C、①③ | D、②④ |
下列关于有机物的描述中正确的是( )
| A、葡萄糖和果糖互为同分异构体,淀粉和纤维素也互为同分异构体 |
| B、利用蛋白质的颜色反应可以鉴别所有的蛋白质 |
| C、多糖、蛋白质、脂肪和聚丙烯等都属于高分子化合物 |
| D、食醋中的主要成分为乙酸,普通食醋中含有3%-5%的乙酸 |
 如图中A、B、C、D是同周期或同主族的相邻元素:
如图中A、B、C、D是同周期或同主族的相邻元素: