题目内容
15.下列有关化学用语使用正确的是( )| A. | 硫原子的原子结构示意图: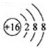 | |
| B. | NH4Cl的电子式: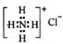 | |
| C. | 原子核内有10个中子的氧原子:${\;}_{8}^{18}O$ | |
| D. | 纯碱的化学式为NaOH |
分析 A.原子结构示意图中,圆圈内数字表示核内质子数,弧线表示电子层,弧线上的数字表示该层上的电子数,质子数等于核外电子数,图示为硫离子结构示意图;
B.氯化铵为离子化合物,复杂阳离子和阴离子均需要括号,图示氯离子书写错误;
C.质量数=质子数+中子数,元素符号的左上角为质量数、左下角为质子数;
D.纯碱指的是碳酸钠,根据化合价书写化学式.
解答 解:A.在原子结构示意图中,圆圈表示原子核,圆圈内的数值为质子数,核外电子层用弧线表示,弧线上的数据表示每层的电子数.
硫原子的质子数是16,原子结构示意图为: ,故A错误;
,故A错误;
B.氯化铵是离子化合物,由氨根离子与氯离子构成,电子式为: ,故B错误;
,故B错误;
C.氧原子的核电荷数为8,原子核内有10个中子的氧原子的质量数为18,该氧原子可以表示为:${\;}_{8}^{18}O$,故C正确;
D.纯碱是碳酸钠,在碳酸钠中,钠元素的化合价是+1,碳酸根的化合价是-2,碳酸钠的化学式是Na2CO3,故D错误;
故选C.
点评 本题考查了有关化学用语规范使用,题目难度不大,注意掌握电子式的概念及表示方法,明确离子化合物与共价化合物的电子式的表示方法及区别,是易错考点.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
5.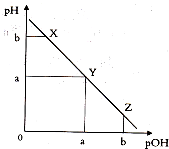 某温度下,向一定体积0.1mol.L一1氨水溶液中逐滴加入等浓度的盐酸,溶液中pOH[pOH=-lgc(OH-)]与pH的变化关系如图所示.下列说法不正确是( )
某温度下,向一定体积0.1mol.L一1氨水溶液中逐滴加入等浓度的盐酸,溶液中pOH[pOH=-lgc(OH-)]与pH的变化关系如图所示.下列说法不正确是( )
 某温度下,向一定体积0.1mol.L一1氨水溶液中逐滴加入等浓度的盐酸,溶液中pOH[pOH=-lgc(OH-)]与pH的变化关系如图所示.下列说法不正确是( )
某温度下,向一定体积0.1mol.L一1氨水溶液中逐滴加入等浓度的盐酸,溶液中pOH[pOH=-lgc(OH-)]与pH的变化关系如图所示.下列说法不正确是( )| A. | 此温度下,水的离子积常数为1.0×l0-2a | |
| B. | X点和Z点所示溶液中H2O的电离程度相同 | |
| C. | X、Y、Z三点所示的溶液中:c(NH4+)+c(H+)═c(Cl-)+c(OH-) | |
| D. | Y点消耗盐酸的体积等于氨水的体积 |
6.已知四种主族元素的离子aWm+、bXn+、cYm-、dZn-具有相同的电子层结构,下列说法正确的是( )
| A. | 若m>n,金属性W>X | |
| B. | 若m>n,气态氢化物的稳定性HmY>HnZ | |
| C. | 若m<n,氧化性Xn+>Wm+ | |
| D. | 若m<n,原子序数a>b>c>d |
10.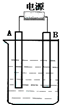 在如图用石墨作电极的电解池中,放入500mL含硫酸铜的溶液进行电解,当电解一会后(时间为t)观察到A电极表面有红色的固态物质生成,B电极有无色气体生成,溶液还是蓝色的;反接电源,再电解相同时间(时间为t),则下列说法正确的是( )
在如图用石墨作电极的电解池中,放入500mL含硫酸铜的溶液进行电解,当电解一会后(时间为t)观察到A电极表面有红色的固态物质生成,B电极有无色气体生成,溶液还是蓝色的;反接电源,再电解相同时间(时间为t),则下列说法正确的是( )
 在如图用石墨作电极的电解池中,放入500mL含硫酸铜的溶液进行电解,当电解一会后(时间为t)观察到A电极表面有红色的固态物质生成,B电极有无色气体生成,溶液还是蓝色的;反接电源,再电解相同时间(时间为t),则下列说法正确的是( )
在如图用石墨作电极的电解池中,放入500mL含硫酸铜的溶液进行电解,当电解一会后(时间为t)观察到A电极表面有红色的固态物质生成,B电极有无色气体生成,溶液还是蓝色的;反接电源,再电解相同时间(时间为t),则下列说法正确的是( )| A. | 一开始A接的是电源的负极 | |
| B. | 反接电源后B电极发生氧化反应 | |
| C. | 反接电源后电解时A电极发生反应的电极反应式4OH--4e-=2H2O+O2↑ | |
| D. | 反接电源后,电解池变成了电镀池,实现了碳(B电极)上镀铜. |
20.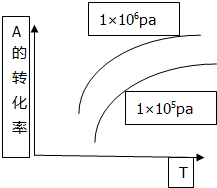 反应mA(g)+B(s)?pC(g)+qD(g)△H>0中A的转化率和温度(T)、压强(P)的关系如图曲线,下列结论正确的是( )
反应mA(g)+B(s)?pC(g)+qD(g)△H>0中A的转化率和温度(T)、压强(P)的关系如图曲线,下列结论正确的是( )
 反应mA(g)+B(s)?pC(g)+qD(g)△H>0中A的转化率和温度(T)、压强(P)的关系如图曲线,下列结论正确的是( )
反应mA(g)+B(s)?pC(g)+qD(g)△H>0中A的转化率和温度(T)、压强(P)的关系如图曲线,下列结论正确的是( )| A. | 逆反应为放热反应m<p+q | B. | 逆反应为吸热反应m>p+q | ||
| C. | 正反应为放热反应m<p+q | D. | 正反应为吸热反应m>p+q |
7.下表是某地区市场上销售的一种“加碘食盐”包装袋上的部分文字说明.请根据此表,结合初中化学和生物学科的知识,回答下列问题.
(1)要在食盐中加碘,是因为碘是人体内合成甲状腺激素的主要原料,缺碘会引起疾病.在人体中,碘是属于微量(选填“常量”或“微量”)元素.
(2)食盐中加碘,这碘指的是元素(填元素、原子或单质).
(3)碘酸钾的化学式为KIO3,其中碘元素的化合价为+5.
(4)根据含碘盐的食用方法可推测碘元素的化学性质,碘酸钾在受热时是分解(容易还是不容易)分解.
| 配料表 | 精制海盐、碘酸钾 |
| 含碘量 | 20~40mg/kg |
| 卫生许可证号 | ××卫碘字(1999)第001号 |
| 分装日期 | 见封底 |
| 储藏方法 | 密封、避光、防潮 |
| 食用方法 | 烹调时,待食品熟后加入碘盐 |
(2)食盐中加碘,这碘指的是元素(填元素、原子或单质).
(3)碘酸钾的化学式为KIO3,其中碘元素的化合价为+5.
(4)根据含碘盐的食用方法可推测碘元素的化学性质,碘酸钾在受热时是分解(容易还是不容易)分解.
5.用于分离两种互不溶性液体的实验操作是( )
| A. | 萃取 | B. | 过滤 | C. | 分液 | D. | 蒸馏 |
 读图题:已知1-丙醇和2-丙醇的结构简式如下:
读图题:已知1-丙醇和2-丙醇的结构简式如下: