题目内容
10. 氯酸钾和亚硫酸氢钾溶液能发生氧化还原反应:
氯酸钾和亚硫酸氢钾溶液能发生氧化还原反应:ClO3-+3HSO3-═3SO42-+Cl-+3H+
已知该反应的速率随c(H+)的增大而加快.
下列为用ClO3-在单位时间内物质的量浓度变化表示的该反应v-t图.下列说法中不正确的是( )
| A. | 反应开始时速率增大可能是c(H+)所致 | |
| B. | 纵坐标为v(Cl-)的v-t曲线与图中曲线完全重合 | |
| C. | 纵坐标为v(H+)的v-t曲线与图中曲线完全重合 | |
| D. | 后期反应速率下降的主要原因是反应物浓度减小 |
分析 由题目信息可知反应的速率随c(H+)的增大而加快;根据电子得失守恒和原子守恒配平方程式,然后根据速率之比等于化学计量数之比可判断v-t曲线与图中曲线是否重合,随着反应的进行,浓度减小,则反应速率减小,以此解答该题.
解答 解:A.由方程式:ClO3-+HSO3--SO42-+Cl-+H+可知:反应开始时随着反应的进行,c(H+)不断增大,反应的速率加快由题目信息可知反应的速率随c(H+)的增大而加快,故A正确;
B.在反应中ClO3-+HSO3--SO42-+Cl-+H+,1molClO3-参加氧化还原反应得到6mol电子,1mol亚硫酸氢根离子参加氧化还原反应失去2mol电子,所以得失电子的最小公倍数是6,则ClO3-的计量数是1,亚硫酸氢根离子的计量数是3,其它原子根据原子守恒来配平,所以该方程式为:ClO3-+3HSO3-=3SO42-+Cl-+3H+,v(ClO3-):v(Cl-)=1:1,纵坐标为v(Cl-)的v-t曲线与图中曲线重合,故B正确;
C.该方程式为:ClO3-+3HSO3-=3SO42-+Cl-+3H+,v(ClO3-):v(H+)=1:3,纵坐标为v(H+)的v-t曲线与图中曲线不重合,故C错误;
D.随着反应的进行,反应物的浓度减少,反应速率减小,所以后期反应速率下降的主要原因是反应物浓度减小,故D正确.
故选C.
点评 本题主要考查了外界条件对化学反应速率的有关知识,为高频考点,侧重于学生的分析、计算能力的考查,难度不大,需要注意的是要抓住题目的信息是解答A选项的关键.

练习册系列答案
相关题目
20.化学反应方程式的理解注重反应过程的研究.下列反应过程中,同时有离子键、极性共价键和非极性共价键的断裂和形成的反应是( )
| A. | Cl2+2NaOH═NaCl+NaClO+H2O | B. | 2Na+2H2O═2NaOH+H2↑ | ||
| C. | CO2+NH3+H2O═NH4HCO3 | D. | 2Na2O2+2CO2═2Na2CO3+O2↑ |
1.下列分子:①BF3,②CCl4,③NH3,④H2O,⑤HCl,⑥CO2.其中只含极性键的非极性分子有( )
| A. | ①②⑥ | B. | ①②⑤ | C. | ②⑤③ | D. | ①②③ |
18.某短周期的非金属元素,其原子核外最外层电子数是内层电子数的一半,则此非金属元素在元素周期表中的位置是( )
| A. | 第二周期第IA族 | B. | 第三周期第IVA族 | C. | 第二周期第VA族 | D. | 第三周期第VA族 |
5.2010年2月19日IUPAC(国际纯粹与应用化学联合会)宣布,第112号化学元素正式名称为“Copernicium”,元素符号为“Cn”,以纪念著名天文学家哥白尼,该元素的一种核素含有的中子数为165.下列关于Cn的说法正确的是( )
| A. | Cn是第六周期元素 | B. | Cn是过渡元素 | ||
| C. | Cn是非金属元素 | D. | Cn的一种核素可表示为165Cn |
15.加热下列各物质没有单质生成的是( )
| A. | KMnO4 | B. | NH3•H2O | C. | HNO3 | D. | H2O2 |
2.下列说法正确的是( )
| A. | 煤干馏得到的煤焦油,其主要用途就是再经蒸馏得到高品质燃油,这一做法可以体现“低碳生活”的理念 | |
| B. | 锅炉水垢中含有的CaSO4,可先用Na2CO3溶液处理,后用酸除去 | |
| C. | 刚玉、红宝石、蓝宝石的主要成分是氧化铝,而青花瓷、石英玻璃、分子筛的主要成分是硅酸盐 | |
| D. | “辽宁舰”上用于舰载机降落拦阻索的特种钢缆,属于新型无机非金属材料 |
19.我国最新报道的高温超导体中,铊是组成成分之一.已知铊与铝是同族元素,关于铊的判断有错误的是( )
| A. | 氢氧化铊是两性氢氧化物 | B. | 铊能置换出盐酸中的氢 | ||
| C. | 铊是质软的银白色的金属 | D. | 铊能生成+3价的化合物 |
1.I.“低碳经济”时代,科学家利用“组合转化”等技术对CO2进行综合利用.
(1)CO2和H2在一定条件下可以生成乙烯:6H2(g)+2CO2(g)+CH2═CH2(g)+4H2O(g)△H=a kJ•mol-1
已知:H2(g)的燃烧热为285.8kJ•mol-1,CH2=CH2(g)的燃烧热为1411.0kJ•mol-1,H2O(g)=H2O(l)△H=-44.0kJ•mol-1,则a=-127.8kJ•mol-1.
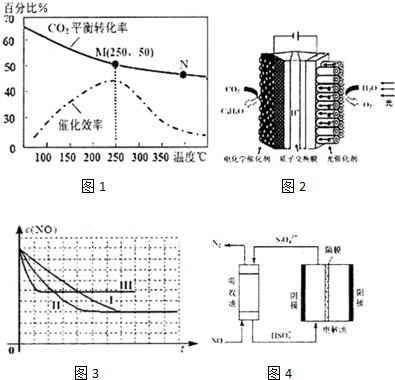
(2)上述生成乙烯的反应中,温度对CO2的平衡转化率及催化剂的催化效率影响如图1,下列有关说法不正确的是①②④(填序号)
①温度越高,催化剂的催化效率越高
②温发低于250℃时,随着温度升高,乙烯的产率增大
③M点平衡常数比N点平衡常数大
④N点正反应速率一定大于M点正反应速率
⑤增大压强可提高乙烯的体积分数
(3)2012年科学家根据光合作用原理研制出“人造树叶”.如图2是“人造树叶”的电化学模拟实验装置图,该装置能将H2O和CO2转化为O2和有机物C3H8O.阴极的电极反应式为:3CO2+18H++18e-=C3H8O+5H2O
II.为减轻大气污染,可在汽车尾气排放处加装催化转化装置,反应方程式为:2NO(g)+2CO(g)?2CO2(g)+N2(g).
(4)上述反应使用等质量的某种催化剂时,温度和催化剂的比表面积对化学反应速率的影响对比实验如下表,c(NO)浓度随时间(t)变化曲线如3图:
①表中a=1.20×10-3.
②实验说明,该反应是放热反应(填“放热”或“吸热”).
③若在500℃时,投料$\frac{c(NO)}{c(CO)}$=1,NO的转化率为80%,则此温度时的平衡常数K=第一种情况:设c(NO)=1mol•L-1,则K=160,
第二种情况:设c(NO)=amol•L-1,则K=$\frac{160}{a}$,
第三种情况:设n(NO)=amol,容器的容积为V L,则K=$\frac{160V}{a}$;.
(5)使用电化学法也可处理NO的污染,装置如图4.已知电解池阴极室中溶液的pH在4~7之间,写出阴极的电极反应式:2HSO3-+2H++2e-=S2O42-+2H2O.吸收池中除去NO的离子方程式为:2NO+2S2O42-+2H2O=N2+4HSO3-.

(1)CO2和H2在一定条件下可以生成乙烯:6H2(g)+2CO2(g)+CH2═CH2(g)+4H2O(g)△H=a kJ•mol-1
已知:H2(g)的燃烧热为285.8kJ•mol-1,CH2=CH2(g)的燃烧热为1411.0kJ•mol-1,H2O(g)=H2O(l)△H=-44.0kJ•mol-1,则a=-127.8kJ•mol-1.
(2)上述生成乙烯的反应中,温度对CO2的平衡转化率及催化剂的催化效率影响如图1,下列有关说法不正确的是①②④(填序号)
①温度越高,催化剂的催化效率越高
②温发低于250℃时,随着温度升高,乙烯的产率增大
③M点平衡常数比N点平衡常数大
④N点正反应速率一定大于M点正反应速率
⑤增大压强可提高乙烯的体积分数
(3)2012年科学家根据光合作用原理研制出“人造树叶”.如图2是“人造树叶”的电化学模拟实验装置图,该装置能将H2O和CO2转化为O2和有机物C3H8O.阴极的电极反应式为:3CO2+18H++18e-=C3H8O+5H2O
II.为减轻大气污染,可在汽车尾气排放处加装催化转化装置,反应方程式为:2NO(g)+2CO(g)?2CO2(g)+N2(g).
(4)上述反应使用等质量的某种催化剂时,温度和催化剂的比表面积对化学反应速率的影响对比实验如下表,c(NO)浓度随时间(t)变化曲线如3图:
| 编号 | T(℃) | NO初始浓度(mol/L) | CO初始浓度(mol/L) | 催化剂的比表面积(m2/g) |
| Ⅰ | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
| Ⅱ | 280 | a | 5.80×10-3 | 124 |
| Ⅲ | 350 | 1.20×10-3 | 5.80×10-3 | b |
②实验说明,该反应是放热反应(填“放热”或“吸热”).
③若在500℃时,投料$\frac{c(NO)}{c(CO)}$=1,NO的转化率为80%,则此温度时的平衡常数K=第一种情况:设c(NO)=1mol•L-1,则K=160,
第二种情况:设c(NO)=amol•L-1,则K=$\frac{160}{a}$,
第三种情况:设n(NO)=amol,容器的容积为V L,则K=$\frac{160V}{a}$;.
(5)使用电化学法也可处理NO的污染,装置如图4.已知电解池阴极室中溶液的pH在4~7之间,写出阴极的电极反应式:2HSO3-+2H++2e-=S2O42-+2H2O.吸收池中除去NO的离子方程式为:2NO+2S2O42-+2H2O=N2+4HSO3-.