题目内容
16.中子数为20的氯原子表示为${\;}_{17}^{37}$Cl.分析 原子符号中左上角的数字表示质量数,左下角数字为质子数,质量数=质子数+中子数,据此书写中子数为20的氯原子符号.
解答 解:原子符号中左上角的数字表示质量数,左下角数字为质子数,氯原子质子数为17,中子数为20的氯原子质量数=质子数+中子数=17+20=37,则表示为:${\;}_{17}^{37}$Cl,
故答案为:${\;}_{17}^{37}$Cl.
点评 本题主要考查了,原子符号的含义以及中子数=质量数-质子数,物质的量的求算,注意有关公式的应用,难度不大.

练习册系列答案
相关题目
7.下列有关碱金属元素铷(Rb)的叙述中,正确的是( )
| A. | 铷与水反应的现象跟钠相似 | |
| B. | 硝酸铷易溶于水 | |
| C. | 在钠、钾、铷三种单质中,铷的熔点最高 | |
| D. | 氢氧化铷是弱碱 |
1.某一元醛发生银镜反应,生成金属银4.32g,取等质量该醛完全燃烧后,可生成水1.08g.则此醛可能是下列中的( )
| A. | 丙醛 | B. | 丙烯醛 | C. | 甲醛 | D. | 丁烯醛 |
8.酯R在稀硫酸,加热的条件下可生成1molHOCH2CH2OH(乙二醇)和2mol羧酸(C5H10O2),则R的结构有( )
| A. | 6种 | B. | 10种 | C. | 12种 | D. | 14种 |
2.下列原子中未成对电子(单独占据1个原子轨道的电子)数为2的是( )
| A. | O | B. | N | C. | Cu | D. | F |
 甲、乙、丙三种化合物均由氢、氮、氧、铜四种元素中的两种组成.常温下,甲是一种含氮质量分数为87.5%的液态化合物,其相对分子质量与空气中某种主要成分的相对分子质量相等;乙和丙是铜的两种常见氧化物,乙是新制氢氧化铜与乙醛反应的还原产物.试回答下列问题:
甲、乙、丙三种化合物均由氢、氮、氧、铜四种元素中的两种组成.常温下,甲是一种含氮质量分数为87.5%的液态化合物,其相对分子质量与空气中某种主要成分的相对分子质量相等;乙和丙是铜的两种常见氧化物,乙是新制氢氧化铜与乙醛反应的还原产物.试回答下列问题: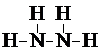 .
.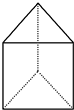 人们对苯及芳香烃的认识有一个不断深化的过程,回答下列问题.
人们对苯及芳香烃的认识有一个不断深化的过程,回答下列问题.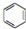 (Ⅱ)
(Ⅱ)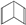
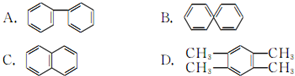
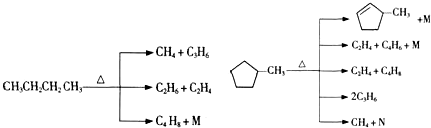
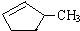 的说法正确的是A.
的说法正确的是A.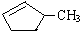 和
和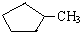
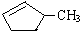 和
和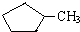 完全燃烧时的耗氧量相同
完全燃烧时的耗氧量相同 可与水以任意比互溶
可与水以任意比互溶