题目内容
13.按要求书写下列反应的化学或离子方程式.(1)在NaOH的环境中,NaI与Cl2反应,每1molNaI完全反应转移6mol电子,写出反应的化学方程式:3Cl2+NaI+6NaOH=NaIO3+6NaCl+3H2O.
(2)等物质的量FeSO4和Na2O2反应,生成Fe(OH)3和其他物质,该反应的离子方程式是4Fe2++4Na2O2 +6H2O=4Fe(OH)3↓+8Na++O2↑.
(3)H2O2和碱性KMnO4溶液反应变为墨绿色溶液,0.25molKMnO4完全反应转移电子的物质的量为0.25mol.该反应的离子方程式是2MnO2+2OH-+H2O2=2MnO42-+O2↑+2H2O.
(4)FeS2在有水存在的条件下用氧气氧化,反应之后得到强酸性溶液,低温下从该强酸性溶液中可得到FeSO4,该氧化还原反应的离子方程式是2FeS2+2H2O+7O2=4H++2Fe2++4SO42-.
(5)在酸性条件下,NaClO加到含Fe2+的溶液中,溶液从浅绿色变成黄色,反应的离子方程式为2Fe2++ClO-+2H+═2Fe3++Cl-+H2O.
(6)在一定条件下,将12gFeS2放入过量的浓硝酸中,反应过程中转移1.5mol电子,该反应的离子方程式是FeS2+14H++15NO3-=F3++2SO42-+15NO2↑+7H20.
(7)取FeSO4溶液,加入淀粉-KI溶液和H2O2,溶液呈蓝色并有红褐色沉淀生成,当消耗2molI-时,共转移3mol电子,该反应的化学方程式是2Fe(SO4)+3H2O2+4KI=2Fe(OH)3↓+2K2SO4+2I2..
分析 (1)在NaOH的环境中,NaI与Cl2反应生成碘酸钠和氯化钠和水;
(2)等物质的量FeSO4和Na2O2反应,生成Fe(OH)3和硫酸钠和氧气;
(3)双氧水与高锰酸钾发生氧化还原反应生成锰酸钾和氧气水;
(4)硫化亚铁被氧化生成硫酸亚铁和氢气;
(5)在酸性条件下,NaClO加到含Fe2+的溶液中,反应生成氯化铁、氯化钠和水;
(6)硫化亚铁被硝酸氧化生成硫酸铁、二氧化氮和水;
(7)双氧水、硫酸亚铁、碘离子发生氧化还原反应生成氢氧化铁、硫酸钾和碘.
解答 解:(1)每1molNaI完全反应转移6mol电子,则I元素的化合价由-1价升高为+5价,生成NaIO3,结合电子守恒可知反应还生成NaCl,化学方程式:3Cl2+NaI+6NaOH=NaIO3+6NaCl+3H2O;
故答案为:3Cl2+NaI+6NaOH=NaIO3+6NaCl+3H2O;
(2)等物质的量FeSO4和Na2O2反应,生成Fe(OH)3和硫酸钠和氧气,离子方程式:4Fe2++4Na2O2 +6H2O=4Fe(OH)3↓+8Na++O2↑;
故答案为:4Fe2++4Na2O2 +6H2O=4Fe(OH)3↓+8Na++O2↑;
(3)双氧水与高锰酸钾发生氧化还原反应生成锰酸钾和氧气水,离子方程式:2MnO2+2OH-+H2O2=2MnO42-+O2↑+2H2O;
故答案为:2MnO2+2OH-+H2O2=2MnO42-+O2↑+2H2O;
(4)硫化亚铁被氧化生成硫酸亚铁和氢气,离子方程式:2FeS2+2H2O+7O2=4H++2Fe2++4SO42-;
故答案为:2FeS2+2H2O+7O2=4H++2Fe2++4SO42-;
(5)在酸性条件下,NaClO加到含Fe2+的溶液中,反应生成氯化铁、氯化钠和水,离子方程式:2Fe2++ClO-+2H+═2Fe3++Cl-+H2O;
故答案为:2Fe2++ClO-+2H+═2Fe3++Cl-+H2O;
(6)硫化亚铁被硝酸氧化生成硫酸铁、二氧化氮和水,离子方程式:FeS2+14H++15NO3-=F3++2SO42-+15NO2↑+7H20;
故答案为:FeS2+14H++15NO3-=F3++2SO42-+15NO2↑+7H20;
(7)双氧水、硫酸亚铁、碘离子发生氧化还原反应生成氢氧化铁、硫酸钾和碘,离子方程式:2Fe(SO4)+3H2O2+4KI=2Fe(OH)3↓+2K2SO4+2I;
故答案为:2Fe(SO4)+3H2O2+4KI=2Fe(OH)3↓+2K2SO4+2I2.
点评 本题考查了化学方程式、离子方程式的书写,侧重考查氧化还原反应方程式书写,明确物质的性质,依据得失电子守恒结合原子个数守恒即可解答,题目难度中等.

 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案| A. | KCN 与KOCN中氮元素的化合价均为-3价 | |
| B. | 氰酸盐被氧化过程中氮和碳的化合价均升高 | |
| C. | 氰酸盐进一步被氧化的产物之一是无毒的N2 | |
| D. | 完全处理含0.1 mol CN-的废水,理论上需要消耗Cl2的体积为5.6L(标准状况下) |


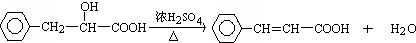 .
. .
. .
. 、
、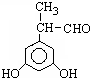 .
. (其中X、Y均部位H)
(其中X、Y均部位H)
 替代,请将Br2与Na2CO3反应的化学方程式补充完整
替代,请将Br2与Na2CO3反应的化学方程式补充完整