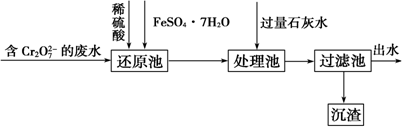
��Ŀ����
2����������ƣ�Na2S2O3����������ͳ����ҵ�Ķ�Ӱ��������ʱ�ظ����εĻ�ԭ����ֽ��Ư��ʱ�����ȼ��ȣ�ij��ѧ̽��С��ͨ���������ϣ�����ͼ1��ʾװ�ü��Լ����Ʊ���������ƣ�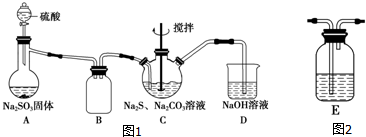
��1��װ��A�еġ����ᡱ���ѡ��C������ĸ��ţ���
A���������� B��Ũ���� C��80%������ D��10%������
��2��װ��C�г�����Ŀ���������������⣬������һ���������壮��װ��C�з�����Ӧ�����ӷ���ʽΪ4SO2+2S2-+CO32-�T3S2O32-+CO2��
��3��װ��B�������Ƿ�ֹװ��C�е�Һ�嵹����װ��A�У�������ȫƿ����װ��D������������β���е�SO2��
��4��������Һ©���е����ỻΪŨ���ᣬװ��C�г���������������⣬������һ�����Σ������εĻ�ѧʽΪNaCl��Ϊ��ֹ�����ε����ɣ���ͬѧ������װ������������ͼ2װ��E����װ��EӦ�����ӵ�λ��ΪA������ĸ��ţ���
A��ֻ����װ��A��װ��B֮��
B��ֻ����װ��B��װ��C֮��
C����װ��A��װ��B��װ��B��װ��C֮�䶼����
D��ֻ����װ��C��װ��D֮��
��װ����ʢ�ŵ��Լ�ΪD������ĸ��ţ���
A��NaOH��Һ B��Na2SO3��Һ C��NaHCO3��Һ D��NaHSO3��Һ��
���� �������������Ʒ�Ӧ����SO2��װ��B�е��������ܾ�Ϊ�̹ܣ�����ȫƿ��װ��C�ж����������ƺ�̼���Ʒ�Ӧ������������ƺͶ�����̼��װ��D�е�����������Һ�������������Ӧ����ֹ��Ⱦ������
��1��SO32-��H+��Ӧ������SO2��������������Ƿ���״̬�����ᣬ�����ܵ����H+��
��2����Ϸ�Ӧ��̼���ƿ�֪���ɵ���������Ϊ������̼����˸÷�Ӧ�ķ�Ӧ��Ϊ�����������ƺ�̼���ƣ�������Ϊ��������ƺͶ�����̼��
��3��װ��B�е��������ܾ�Ϊ�̹ܣ�����ȫƿ��װ��D�е�����������Һ�������������Ӧ��
��4���������ỻΪŨ���ᣬ�����ɵĶ��������л��� HCl��װ�� E �������dz�ȥ HCl������Ӧ�����ڰ�ȫƿǰ�� �����������������ơ��������ơ�̼��������Һ���ܷ�����Ӧ��
��� �⣺�������������Ʒ�Ӧ����SO2��װ��B�е��������ܾ�Ϊ�̹ܣ�����ȫƿ��װ��C�ж����������ƺ�̼���Ʒ�Ӧ������������ƺͶ�����̼��װ��D�е�����������Һ�������������Ӧ����ֹ��Ⱦ������
��1��SO32-��H+��Ӧ������SO2��������������Ƿ���״̬�����ᣬ�����ܵ����H+�������Ũ�ȴ���Ӧ���ʿ죬��ѡȡ80%�����ᣬ
�ʴ�Ϊ��C��
��2����Ϸ�Ӧ��̼���ƿ�֪���ɵ���������Ϊ������̼����˸÷�Ӧ�ķ�Ӧ��Ϊ�����������ƺ�̼���ƣ�������Ϊ��������ƺͶ�����̼�����ӷ���ʽΪ��4SO2+2S2-+CO32-�T3S2O32-+CO2��
�ʴ�Ϊ��4SO2+2S2-+CO32-�T3S2O32-+CO2��
��3��װ��B�е��������ܾ�Ϊ�̹ܣ�����ȫƿ��װ��D�е�����������Һ�������������Ӧ����ֹ��Ⱦ������
�ʴ�Ϊ����ֹװ��C�е�Һ�嵹����װ��A�У�������ȫƿ��������β���е�SO2��
��4���������ỻΪŨ���ᣬ�����ɵĶ��������л��� HCl��HCl ����̼���ơ����Ʒ�Ӧ�����Ȼ��ƣ�װ�� E �������dz�ȥ HCl������Ӧ�����ڰ�ȫƿǰ�� �����������������ơ��������ơ�̼��������Һ���ܷ�����Ӧ�����ֻ��ѡȡ NaHSO3��Һ��
�ʴ�Ϊ��NaCl��A��D��
���� ���⿼���������Ʊ�ʵ�鷽������ƺ��Ʊ����̷���Ӧ�ã���Ҫ��ʵ�����������Ӧ�ã����ջ�����ע������ǽ���ؼ�����Ŀ�Ѷ��еȣ�

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�| A�� | ����NH4HSO4���壬v��H2������ | B�� | ����������������Һ��v��H2����С | ||
| C�� | ����CH3COONa���壬v��H2������ | D�� | �μ�����CuSO4��Һ��v��H2����С |
| A�� | Mg2+ | B�� | Fe3+ | C�� | Na+ | D�� | Na+ |
| A�� | n-2 | B�� | n | C�� | n-1 | D�� | 2n |
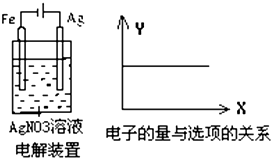
| A�� | Ag+���ʵ���Ũ�� | B�� | NO3-���ʵ���Ũ�� | ||
| C�� | ��Һ��pH | D�� | ���������� |

 ��1��Ԫ��M�Ƕ�����Ԫ�أ��䳣�������ں�ˮ�У����ʱ���Ϊ��������������
��1��Ԫ��M�Ƕ�����Ԫ�أ��䳣�������ں�ˮ�У����ʱ���Ϊ�������������� ��
��