题目内容
20mL 0.5mol/L某酸溶液跟10mL 2mol/L NaOH溶液恰好反应生成正盐,则该酸不可能是( )
| A、HCl |
| B、H2SO4 |
| C、H2C2O4(草酸) |
| D、H3PO4 |
考点:化学方程式的有关计算
专题:计算题
分析:根据n=cV计算酸、NaOH的物质的量,酸、碱反应本质:H++OH-=H2O,据此计算该为几元酸,结合选项判断.
解答:
解:酸的物质的量=0.02L×0.5mol/L=0.01mol,NaOH的物质的量=0.01L×2mol/L=0.02mol,
令酸为n元酸,酸、碱反应本质:H++OH-=H2O,则:0.01mol×n=0.02mol,解得n=2,故该酸为二元酸,
HCl为一元酸,硫酸、草酸都是二元酸,磷酸是三元酸,该酸不可能为HCl、H3PO4,
故选AD.
令酸为n元酸,酸、碱反应本质:H++OH-=H2O,则:0.01mol×n=0.02mol,解得n=2,故该酸为二元酸,
HCl为一元酸,硫酸、草酸都是二元酸,磷酸是三元酸,该酸不可能为HCl、H3PO4,
故选AD.
点评:本题考查化学方程式有关计算,比较基础,明确酸、碱反应的本质是关键,侧重对基础知识的巩固.

练习册系列答案
 作业辅导系列答案
作业辅导系列答案 同步学典一课多练系列答案
同步学典一课多练系列答案
相关题目
常温下,下列溶液中的微粒浓度关系正确的是( )
A、在0.1mo1/L Na2CO3溶液中:c(Na+)+c(H+)=c(C
| ||||
| B、pH相等的①NH4Cl②(NH4)2SO4③NH4HSO4溶液中,c(NH4+)大小顺序:①=②>③ | ||||
| C、pH=11的氨水与pH=3的盐酸等体积混合:c(Cl-)=c(NH4+)>c(OH-)=c(H+) | ||||
| D、0.2mol?L-1CH3COOH溶液与0.1mol?L-1NaOH溶液等体积混合:2c(H+)-2c(OH-)=C(CH3COO-)-C(CH3COOH) |
从硫化物中提取单质锑(Sb)是先在高温下将硫化物转化为氧化物,再用碳还原:
①2Sb2S3+3O2+6Fe→Sb4O6+6FeS ②Sb4O6+6C→4Sb+6CO↑
Sb2S3和Sb4O6中Sb都为+3价.下列叙述正确的是( )
①2Sb2S3+3O2+6Fe→Sb4O6+6FeS ②Sb4O6+6C→4Sb+6CO↑
Sb2S3和Sb4O6中Sb都为+3价.下列叙述正确的是( )
| A、反应①中的氧化剂是Sb2S3 |
| B、反应②中还原剂是Sb4O6 |
| C、反应①中每生成3 mol FeS,转移6 mol电子 |
| D、反应②说明高温下C的还原性比Sb强 |
下列对“物质的量”“摩尔”的叙述不正确的是( )
| A、物质的量是一个物理量,它表示含有一定数目粒子的集体 |
| B、摩尔是物质的量的单位,用于表示物质所含微观粒子的多少 |
| C、摩尔是用来量度物质含有一定数目粒子的集体的多少的单位 |
| D、摩尔既能用来计量纯净物,又能用来计量混合物 |
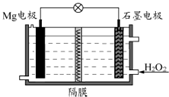 Mg-H2O2电池可用于驱动无人驾驶的潜航器.该电池以海水为电解质溶液,示意图如下.该电池工作时,下列说法不正确的是( )
Mg-H2O2电池可用于驱动无人驾驶的潜航器.该电池以海水为电解质溶液,示意图如下.该电池工作时,下列说法不正确的是( )| A、Mg 电极是该电池的负极 |
| B、H2O2 在石墨电极上发生还原反应 |
| C、石墨电极附近溶液的pH 增大 |
| D、溶液中Cl-向正极移动 |
下列说法正确的是( )
| A、pH=2的盐酸与pH=l的硫酸溶液中c(H+)之比为2:1 |
| B、pH=3的醋酸溶液与pH=11的NaOH溶液等体积混合,则c(Na+)+c(H+)=c(OH-)+c(CH3COO-) |
| C、pH=6的醋酸用水稀释100倍,PH=8 |
| D、在25 mL 0.1 mol?L-1NaOH溶液中,滴入0.1 mol?L-1的CH3COOH溶液至混合溶液pH=7时,则滴加CH3COOH溶液的体积大于25 mL |
NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、标准状况下,22.4L二氯甲烷的分子数约为NA个 |
| B、常温下,在18g18O2中含有NA个氧原子 |
| C、1.0L 1.0mo1?L-1的NaAlO2水溶液中含有的氧原子数为2NA |
| D、25℃时pH=13的NaOH溶液中含有OH一的数目为0.1NA |
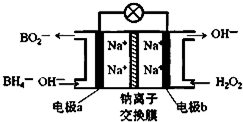 某新型电池NaBH4(其中B的化合价为+3价)和H2O2作原料,该电池可用作深水勘探等无空气环境的电源,其工作原理如图所示.下列说法正确的是( )
某新型电池NaBH4(其中B的化合价为+3价)和H2O2作原料,该电池可用作深水勘探等无空气环境的电源,其工作原理如图所示.下列说法正确的是( )| A、电池工作时Na+从b极区移向a极区 |
| B、b极上的电极反应式为:H2O2+2e-+2H+═2H2O |
| C、每消耗3molH2O2,转移3mol e- |
| D、a极上的电极反应式为:BH4-+8OH--8e-═BO2-+6H2O |