题目内容
下列物质既含离子键又含共价键的是( )
| A、NO2 |
| B、MgC12 |
| C、HCl |
| D、NaOH |
考点:化学键
专题:
分析:一般来说,活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,第IA、IIA族元素和第VIA、VIIA族元素之间易形成离子键.
解答:
解:A.二氧化氮分子中氮原子和氧原子之间存在共价键,故A错误;
B.氯化镁中镁离子和氯离子之间存在离子键,故B错误;
C.氯化氢中氯原子和氢原子之间存在共价键,故C错误;
D.氢氧化钠中钠离子和氢氧根离子之间存在离子键,氢原子和氧原子之间存在共价键,故D正确;
故选D.
B.氯化镁中镁离子和氯离子之间存在离子键,故B错误;
C.氯化氢中氯原子和氢原子之间存在共价键,故C错误;
D.氢氧化钠中钠离子和氢氧根离子之间存在离子键,氢原子和氧原子之间存在共价键,故D正确;
故选D.
点评:本题考查了化学键的判断,根据物质中微粒之间形成的化学键结合基本概念来分析解答,题目难度不大.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案
相关题目
HA为酸性略强于醋酸的一元弱酸.在0.1mol?L-1 NaA溶液中,离子浓度关系正确的是( )
| A、c(Na+)>c(A-)>c(H+)>c(OH-) |
| B、c(Na+)>c(OH-)>c(A-)>c(H+) |
| C、c(Na+)+c(OH-)=c(A-)+c(H+) |
| D、c(Na+)+c(H+)=c(OH-)+c(A-) |
称取两份铝粉,第一份加入足量的NaOH溶液中,第二份加入足量的盐酸中,若放出H2的体积相同(同温同压),则两份铝粉的质量比为( )
| A、1:2 | B、1:3 |
| C、3:2 | D、1:1 |
已知:2NO2(g)
2NO(g)+O2(g)△H<0,下列关于该反应的示意图或描述不正确的是( )
| 催化剂 |
| 加热 |
A、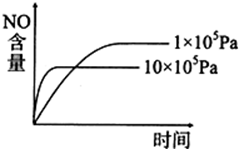 |
B、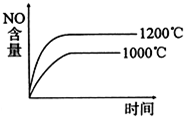 |
| C、NO难溶于水,可以用排水法收集,但不可以用排空气法 |
| D、当生成标准状况下3.36L的氧气时,该反应转移0.6mole |
已知NaHSO4在水中的电离方程式为:NaHSO4═Na++H++SO42-.某温度下,向c(H+)=1×10-6mol/L的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液中的c(H+)=1×10-2 mol/L.下列对该溶液的叙述错误的是( )
| A、该温度高于25℃ |
| B、由水电离出来的H+的浓度为1×10-10 mol/L |
| C、NaHSO4晶体的加入抑制了水的电离 |
| D、取该溶液加水稀释100倍,溶液中的c(OH-)减小 |
下列离子方程式书写正确的是( )
| A、浓烧碱溶液中加入铝片:Al+2OH-═AlO2-+H2↑ |
| B、石灰石溶于醋酸:CaCO3+2CH3COOH=2CH3COO-+Ca2++CO2↑+H2O |
| C、Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-═2Fe2++I2 |
| D、NH4HCO3溶于过量的NaOH溶液中:HCO3-+OH-=CO32-+H2O |
当可逆反应2SO2+O2?2SO3达到平衡经通入18O2,再次达到平衡时,18O存在于( )
| A、SO2、O2 |
| B、SO2、SO3 |
| C、SO2、SO3、O2 |
| D、SO3、O2 |
下列有关化学用语使用正确的是( )
A、NH4Br的电子式: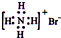 | ||
B、S的结构示意图: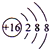 | ||
| C、乙酸的分子式:CH3COOH | ||
D、原子核内有l8个中子的氯原子:
|